Willkommen auf der Homepage des Arbeitskreises von Prof. C. Schneider. Hier finden Sie Informationen zu unseren Veröffentlichungen.
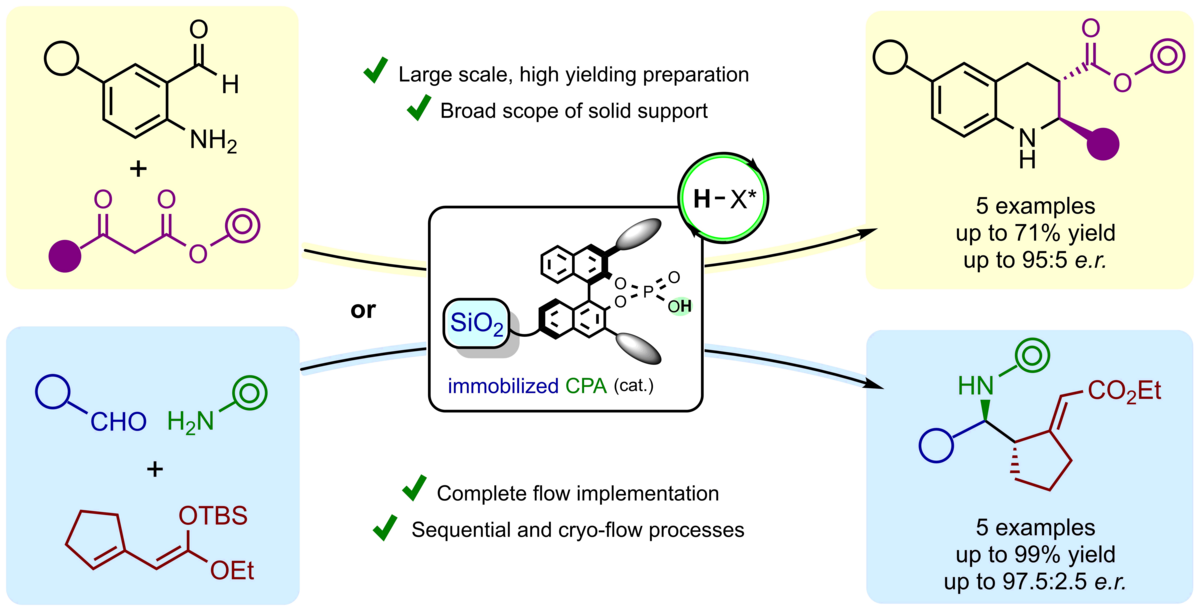
160. Ein allgemeiner, modularer Zugang zu immobilisierten chiralen Phosphorsäurekatalysatoren und deren Anwendung in Durchflussprozessen
M. Laue, M. Schneider, M. Gebauer, W. Böhlmann, R. Gläser, C. Schneider
Inhalt: In dieser Arbeit wurde die direkte Immobilisierung von chiralen Phosphorsäurekatalysatoren (CPAs) auf eine Vielzahl von festen Trägern wie Siliziumdioxid, Polystyrol und Aluminiumoxid realisiert. Diese heterogenen Katalysatoren wurden in hoher Ausbeute hergestellt und durch Elementanalyse mittels ICP-OES, Stickstoffsorptionsmessungen, thermogravimetrische Analyse, STEM/EDX-Bilder und Festkörper-NMR-Spektroskopie eingehend charakterisiert. Darüber hinaus wurden die immobilisierten Katalysatoren für eine Vielzahl synthetisch wertvoller, hoch stereoselektiver Transformationen unter Batch- und Durchflussbedingungen eingesetzt, darunter Transferhydrierungen, eine Friedländer-Kondensation/Transferhydrierungssequenz und Mannich-Reaktionen unter kryogenen Durchflussbedingungen. Im Allgemeinen wurden hohe Ausbeuten und Stereoselektivitäten sowie eine robuste Stabilität und Wiederverwendbarkeit des Katalysators beobachtet. Nach 10 Durchläufen unter Batch-Bedingungen wurde kein Verlust an Selektivität oder katalytischer Aktivität festgestellt. Unter kontinuierlichen Durchflussbedingungen war das heterogene System 19 Stunden lang in Betrieb und die hohe Enantioselektivität blieb während des gesamten Prozesses unverändert. Dieses neue Konzept kann daher die Anwendbarkeit von CPAs speziell im Hinblick auf den umweltfreundlicheren und ressourceneffizienteren Einsatz in Durchflussprozessen auf ein höheres Niveau heben. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
ACS Catal. 2024, 14, 5550-5559. Publikation lesen
159. Organokatalysierte enantioselektive oxa-Piancatelli Umlagerung
R. Sarkar, A. Korell., C. Schneider
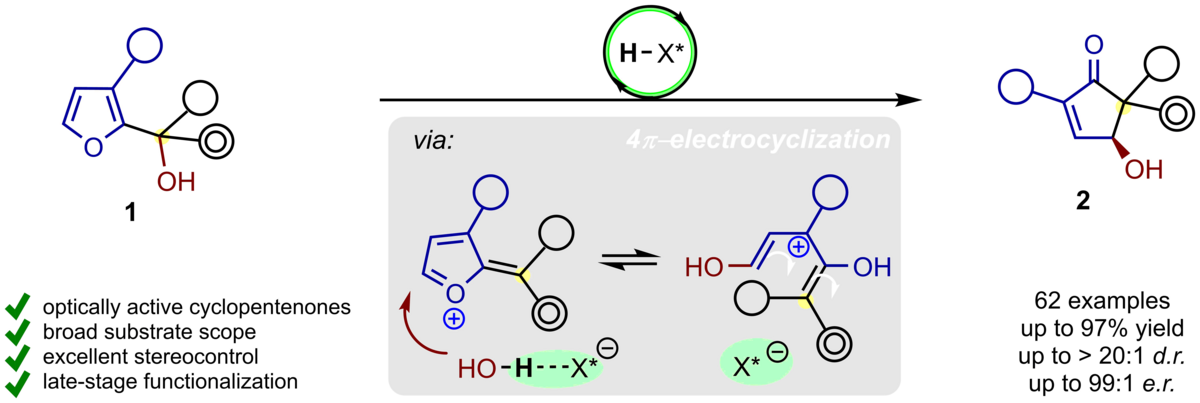
Inhalt: Es wurde die erste hochenantioselektive Oxa-Piancatelli-Umlagerung entwickelt. Dieser Prozess wird durch eine chirale, von BINOL abgeleitete Phosphorsäure katalysiert und lagert eine breite Palette von Furylcarbinolen 1 in hoch-substituierte γ-Hydroxycyclopentenone 2 in hoher Ausbeute mit ausgezeichneten Diastereo- und Enantioselektivitäten (bis zu 99:1 er) um. Diese Reaktion weist dabei eine hohe Toleranz gegenüber weiteren funktionellen Gruppen auf und wurde auch auf komplexe bioaktive Moleküle angewendet. Die Produkte 2 wurden zudem zu wertvollen molekularen Gerüsten umgesetzt, was ihre Vielseitigkeit und ihren synthetischen Nutzen unterstreicht. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Chem. Commun. 2024, 60, 3063–3066. Publikation lesen
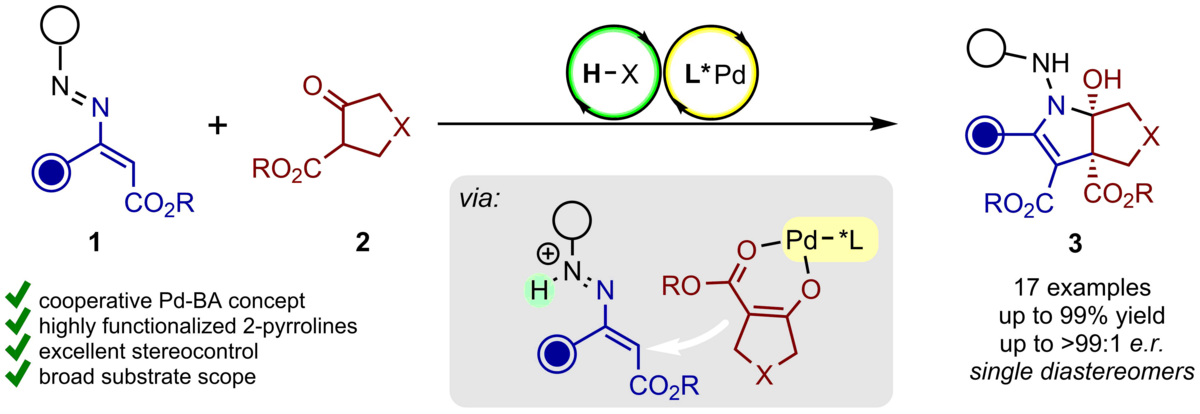
158. Enantioselektive (3+2)-Annellierung von ß-Keto-Estern mit Azoalkenen zu bicyclischen Dihydropyrrolen durch kooperative Palladium- und Brønsted-Säure-Katalyse
T. Friedmann, D. A. Mireles-Chávez, F. L. Walter, C. Schneider
Inhalt: Eine kooperative Palladium- und Brønsted-Säure-Katalyse ermöglichte die asymmetrische konjugierte Addition von cyclischen ß-Ketoestern 2 an Azoalkene 1, bei der eine abschließende Hemiaminalbildung die formale (3+2)-Annellierung komplettierte. Diese Transformation wurde durch den Einsatz chiraler Pd-Aqua-Komplexe als kombinierte Brønsted-Säure-Base-Katalysatoren realisiert. Auf diese Weise wurden bicyclische und hochfunktionalisierte Dihydropyrrole 3 mit zwei benachbarten quaternären stereogenen Zentren in ausgezeichneter Ausbeute als einzelne Diastereomere und mit außergewöhnlicher Enantioselektivität gebildet. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Eingeladener Artikel im Rahmen des Themenclusters "Chemical Synthesis and Catalysis in Germany"
Synlett 2024, 35, 997-1000. Publikation lesen
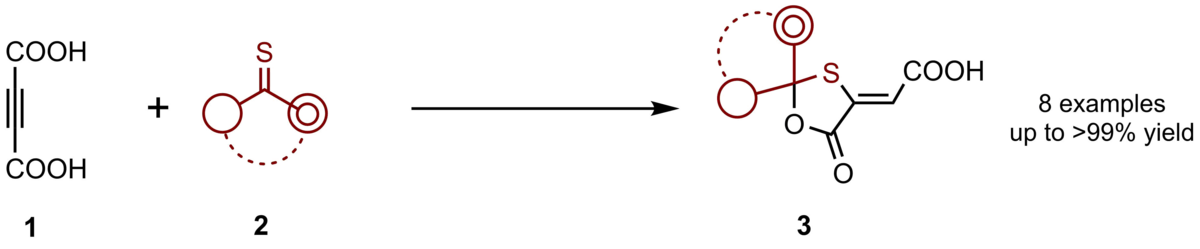
157. Direkter Zugang zu 1,3-Oxathiolan-5-onen durch (3+2)-Cycloaddition von Thioketonen und Acetylendicarbonsäure
F. Sachse, C. Schneider
Inhalt: 1,3-Oxathiolan-5-one sind eine bisher nur wenig untersuchte Klasse von Schwefelheterozyklen, von denen sich einige als wichtige Vorstufen für HIV-Medikamente oder bioaktive, antikarzinogene Verbindungen erwiesen haben. Es wurde ein neuartiges und effektives Verfahren für die direkte Erzeugung dieses Strukturmotivs in einer (3+2)-Cycloaddition von Thioketonen und Acetylendicarbonsäure entwickelt. Die Produkte der Cycloaddition wurden mit vollständiger Regioselektivität und in einer Ausbeute von bis zu 99 % erhalten. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Dieses Manuskript ist Teil einer Sondersammlung des Indo-German Workshop (IGW)
Eur. J. Org. Chem. 2023, e202300834. Publikation lesen
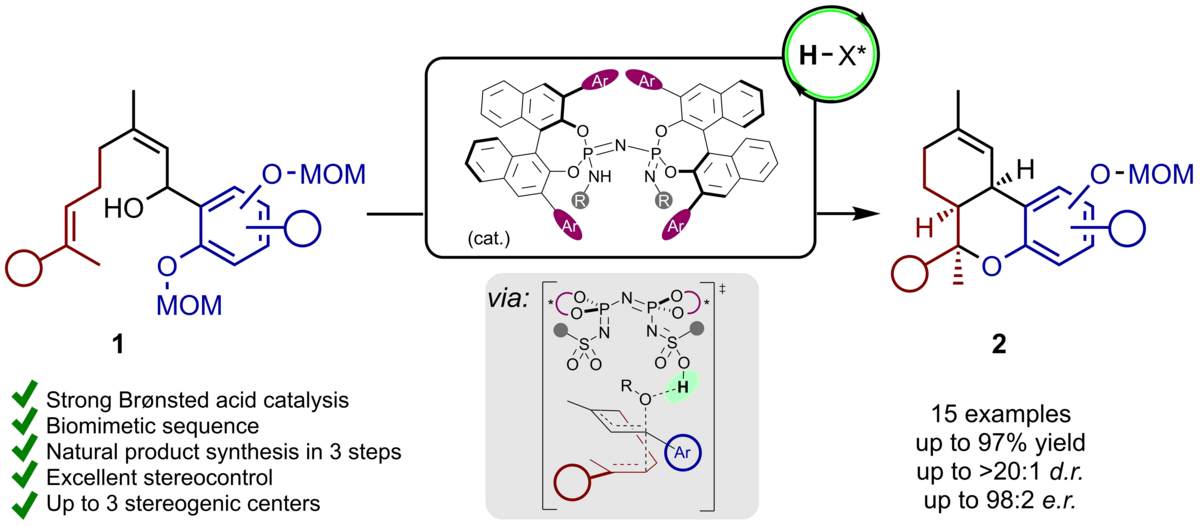
156. Brønsted-Säure-katalysierte asymmetrische Synthese von cis-Tetrahydrocannabinoiden
C. Dorsch, C. Schneider
Inhalt: In einer katalytischen, asymmetrischen Cyclisierung von 1-Arylterpenolen können in einem einzigen Schritt optisch aktive cis-Tetrahydrocannabinoid-Gerüste aufgebaut werden. Als optimale chirale Katalysatoren wurden die stark sauren Imidodiphosphorimidate (IDPis) identifiziert, die die Produkte mit guten Ausbeuten und ausgezeichneter Enantioselektivität liefern. Nach der MOM-Entschützung wurden einige natürlich vorkommende Cannabimimetika wie (–)-cis-Δ9-Tetrahydrocannabinol und (–)-Perrotettinen sowie einige unnatürliche Analoga entlang einer lediglich dreistufigen biomimetischen Sequenz zugänglich gemacht. (Frei übersetzter Titel und Abstract)
Angew. Chem. 2023, e202302475. PUBLIKATION lesen
Angew. Chem. Int. Ed. 2023, e202302475. PUBLIKATION lesen
ChemRxiv., 2023. Preprint-Veröffentlichung lesen
Gewürdigt: in Synfacts 2023, 19, 0820. PUBLIKATION lesen
Kommentiert: in "Alkaloid Synthesis" (D. F. Taber) 2023. KOMMENTAR Lesen
Pressemitteilung 2023/088 vom 17.05.2023 der Universität Leipzig zu Forschende entwickeln neue Methode zur Synthese eines Cannabispflanzen-Wirkstoffs lesen
155. Neueste Entwicklungen auf dem Gebiet der chiralen Palladium-aqua-Komplexe als kooperative Brønsted Säure-Base-Katalyse in der organischen Synthese
C. Gärtner, C. Schneider
Inhalt: Chirale Diphosphan-Pd-aqua-Komplexe wurden aufgrund ihrer außergewöhnlichen Reaktivität als kooperative Brønsted-Säure-Base-Katalysatoren in einer Vielzahl von asymmetrischen Transformationen erfolgreich eingesetzt. Die Besonderheit dieser Katalysatoren beruht auf der Generierung von chiralen und nucleophilen Pd-Enolaten durch eine Deprotonierung von β-Dicarbonylverbindungen und der gleichzeitigen Aktivierung von Elektrophilen durch die aus dem Katalysator freigesetzte Brønsted-Säure. Ursprünglich wurden diese Katalysatoren von der Sodeoka-Gruppe vor etwa 25 Jahren etabliert, allerdings wurden nach den anfänglichen Berichten in den frühen 2000er Jahren für eine längere Zeit keine weiteren Publikationen auf diesem Gebiet veröffentlicht. In den letzten Jahren gab es jedoch neue Entwicklungen zur enantioselektiven Synthese von verschiedenen Heterocyclen und anderen nützlichen Strukturmotiven, die von den einzigartigen Eigenschaften der chiralen Pd-Aqua-Komplexe profitierten. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
ChemCatChem 2023, e202300343. Publikation lesen
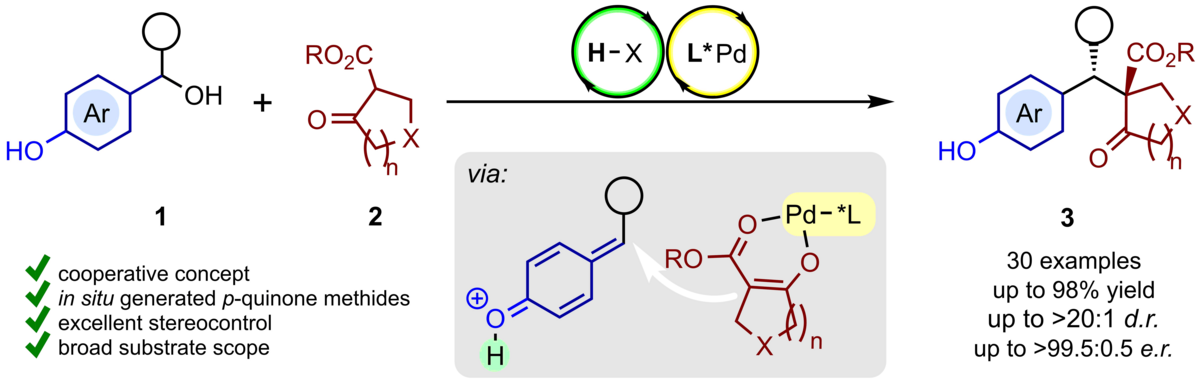
154. Enantioselektive 1,6-Addition von β-Ketoester-Enolaten an in situ erzeugte para-Chinonmethide durch kooperative Palladium- und Brønsted-Säure-Katalyse
C. V. Gärtner, C. Schneider
Inhalt: Eine enantioselektive 1,6-Addition von β-Ketoestern an in situ erzeugte para-Chinonmethide wurde durch chirale Pd-Aqua Komplexe basierend auf dem Konzept der kooperativen Palladium/Brønsted-Säure-Katalyse realisiert. Exzellente Ausbeuten, eine hervorragende Enantiokontrolle und gute Diastereoselektivität zusammen mit einer hohen Substratbreite sind die herausragenden Schlüsselfaktoren dieser Transformation. Die Bedeutung dieser Reaktion wird außerdem durch ein einfaches Up-Scaling und anschließende komplexitätssteigernde Modifikationen unterstrichen. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Org. Lett. 2023, 25, 416-420. Publikation lesen
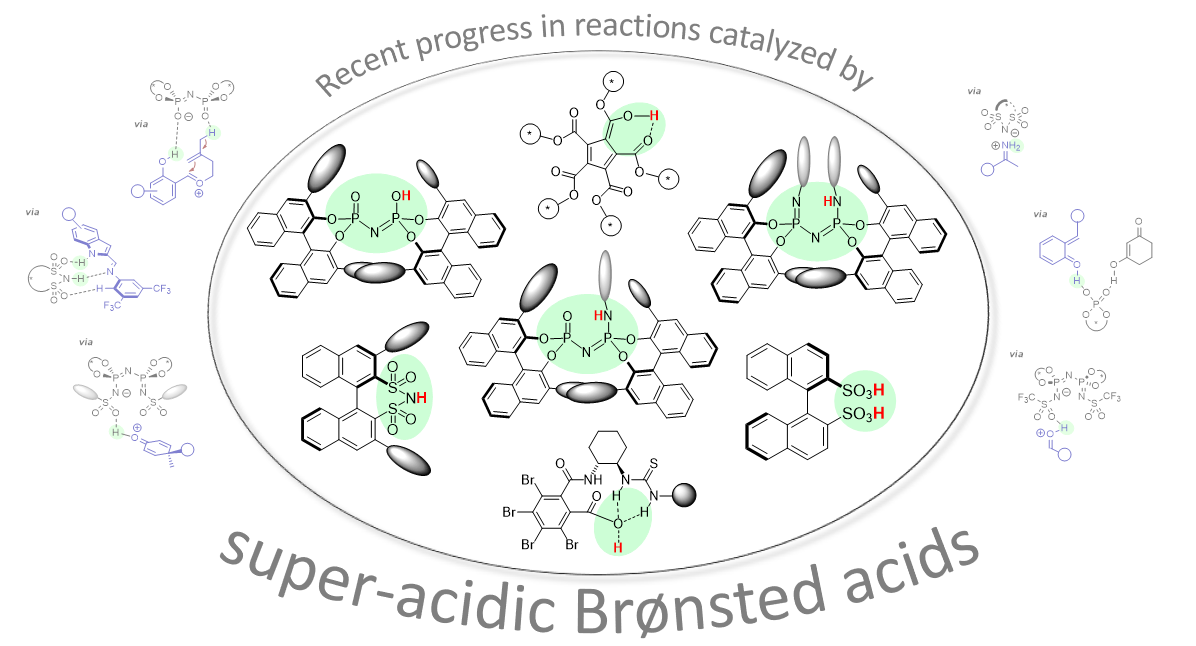
153. Neue Entwicklungen in der enantioselektiven Brønsted Säurekatalyse mit starken Wasserstoffbrückendonoren in der asymmetrischen Organokatalyse: Neue Strategien, Katalysatoren und Möglichkeiten
C. Dorsch, C. Schneider
Inhalt: In den letzten zwei Jahrzehnten hat sich die chirale Brønsted-Säurekatalyse stürmisch entwickelt. Ausgehend von den bahnbrechenden Beiträgen von Akiyama und Terada zu BINOL-Phosphorsäuren wurden dieses und verwandte chirale Motive stetig modifiziert und zu immer saureren und gleichzeitig zu hochselektiven chiralen Katalysatoren verbessert. Fast jede Reaktion, die einer sauren Katalyse unterliegt, kann heutzutage enantioselektiv mit guter Enantiokontrolle durchgeführt werden. Während die ursprünglichen Akiyama/Terada-Katalysatoren weitestgehend auf basische Substrate wie Imine beschränkt waren, können die in diesem Kapitel beschriebenen neueren Katalysatoren problemlos normale Carbonylsubstrate, Alkohole und sogar Olefine aktivieren. Frühere Einschränkungen, die sich aus hohen Katalysatorbeladungen und Problemen beim Upscaling ergaben, wurden weitgehend mit der neuesten Generation von supersauren Brønsted-Säurekatalysatoren überwunden, die häufig mit sehr niedrigen Katalysatorbeladungen von bis zu 0,01 Mol-% arbeiten und daher höchst effektiv mit den leistungsstärksten Metallkatalysatoren konkurrieren. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
(L. Albrecht, Ed.), Wiley-VCH 2023, 1, 3-42, Online ISBN: 9783527832217, DOI:10.1002/9783527832217.
152. Enantioselektive [6+2]-Cycloaddition von transienten 3-Methid-3H-pyrrolen mit 2-Vinylindolen unter chiraler Brønsted-Säure-Katalyse
R. Sarkar, I. Kallweit, C. Schneider
Inhalt: Eine organokatalytische [6+2]-Cycloaddition von 3-Methid-3H-pyrrolen mit 2-Vinylindolen gelingt unter BINOL-Phosphorsäure-Katalyse hoch diastereo- and enantioselektiv und liefert komplexe Cyclopenta[b]pyrrole. Die drei benachbarte stereogene Zentren tragenden Heterocyclen werden dabei in guten Ausbeuten, als einheitliche Diastereomere und mit hoher Enantioselektivität erhalten. Als Substrate werden Pyrrol-3-carbinole verwendet und unter Phosphorsäure-Katalyse in die transienten 3-Methid-3H-pyrrole überführt. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Org. Lett. 2022, 24, 6433–6437. Publikation lesen
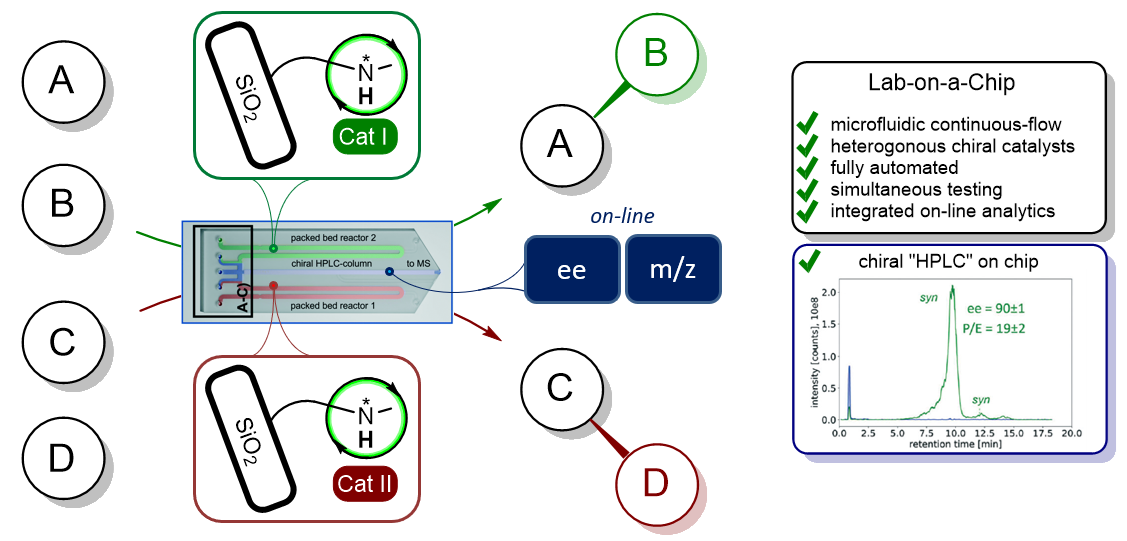
151. Ein hochfunktionalisierter ressourceneffizienter mikrofluidischer Chip für die parallel ablaufende Untersuchung von immobilisierten chiralen Katalysatoren im kontinuierlichen Durchflussverfahren via miniaturisierte LC/MS-Analyse
H. Westphal, R. Warias, C. Weise, D. Ragno, H. Becker, M. Spanka, A. Massi, R. Gläser, C. Schneider, D. Belder
Inhalt: Ein hochfunktionalisierter mikrofluidischer Chip wird für die parallel ablaufende Untersuchung von stereoselektiven, heterogen-katalysierten Reaktionen vorgestellt. Erstmals werden mehrere Festbett-μ-Flow-Reaktoren mit einer chiralen Trenneinheit auf einem Chip kombiniert, der nahtlos mit der Massenspektrometrie verbunden ist. Durch die Entwicklung eines automatisierten Aufbaus ermöglicht dieser Ansatz die Untersuchung der Leistungsfähigkeit verschiedener Katalysatoren in einem einzigen Durchlauf. Auf diese Weise ist ein vollautomatisiertes quasi-simultanes Testen von zwei Festbettreaktoren bezüglich Enantioselektivität und Umsatz möglich, verbunden mit einem deutlich geringeren Ressourceneinsatz im Vergleich zu klassischen Rohrreaktor-HPLC-MS-Systemen. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
React. Chem. Eng., 2022, 7, 1936-1944. Publikation lesen
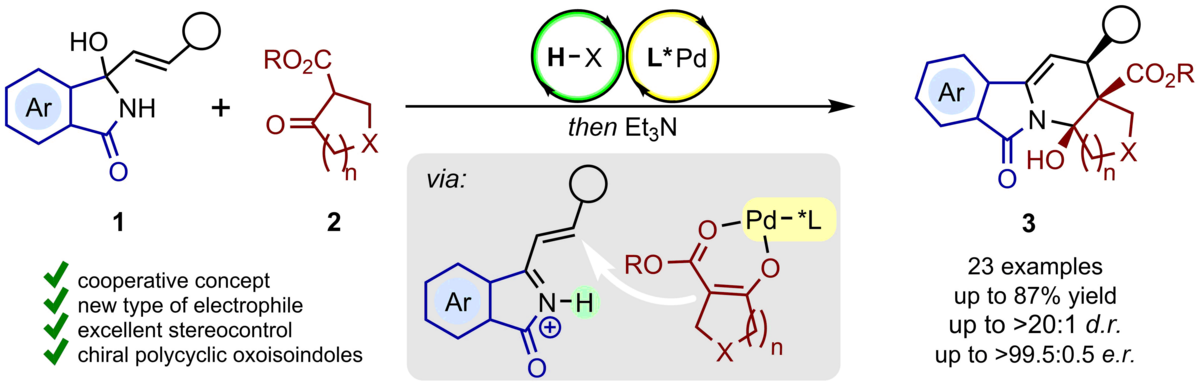
150. Enantioselektive Anellierung von α,β-ungesättigten N-Acyliminium-Ionen mit β-Ketoester-Enolaten durch kooperative Palladium/Brønsted-Säure-Katalyse
C. V. Gärtner, C. Schneider
Inhalt: Die erste enantioselektive Anellierung von in situ erzeugten α,β-ungesättigten N-Acyliminium-Ionen mit chiralen Metall-Enolaten wurde durch eine kooperative Palladium/Brønsted-Säure-Katalyse realisiert. Damit wurde ein wertvoller Zugang zu neuartigen polycyclischen Oxoisoindolen mit drei benachbarten stereogenen Zentren ermöglicht, die typischerweise in guten Ausbeuten, in hervorragender Enantioselektivität (bis zu >99:1 e.r.) und moderater bis guter Diastereoselektivität erhalten wurden. Die Praktikabilität des Verfahrens wurde durch ein Up-Scaling sowie durch die weitere Umsetzung in synthetisch wertvolle Verbindungen eindrucksvoll demonstriert. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Org. Lett. 2022, 24, 3560-3564. Publikation lesen
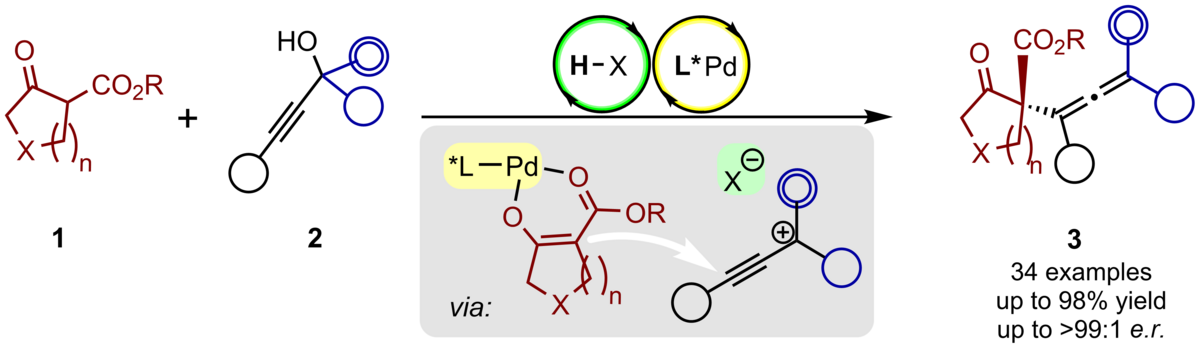
149. Kooperative Palladium/Brønsted Säure-Katalyse für die enantioselektive Allenylierung von β-Ketoestern
H. J. Loui, C. Schneider
Inhalt: Unter kooperativer Pd/Brønsted-Säure-Katalyse gelingt die erste enantioselektive Allenylierung von Pd-Enolaten durch die Reaktion von ß-Ketoestern mit Propargylalkoholen. Die Reaktion verläuft über einen offenen Übergangszustand, wobei die Enantioinduktion ausschließlich durch ein in situ erzeugtes, chirales Metallenolat erfolgt und somit keine weiteren Wechselwirkungen zwischen Elektrophil und Katalysator benötigt werden. Damit komplementiert diese Methode literaturbekannte Ansätze, infolgedessen eine große Substratbreite mit bis dato nicht zugänglichen Substraten etabliert werden konnte. Im Rahmen dieser Reaktion wurden die Produkte in sehr guten Ausbeuten und exzellenten Enantioselektivitäten (bis zu 99:1 e.r.) erhalten. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Org. Lett. 2022, 24, 1496-1501. Publikation lesen
Gewürdigt: in Synfacts 2022, 18, 0508. Publikation Lesen
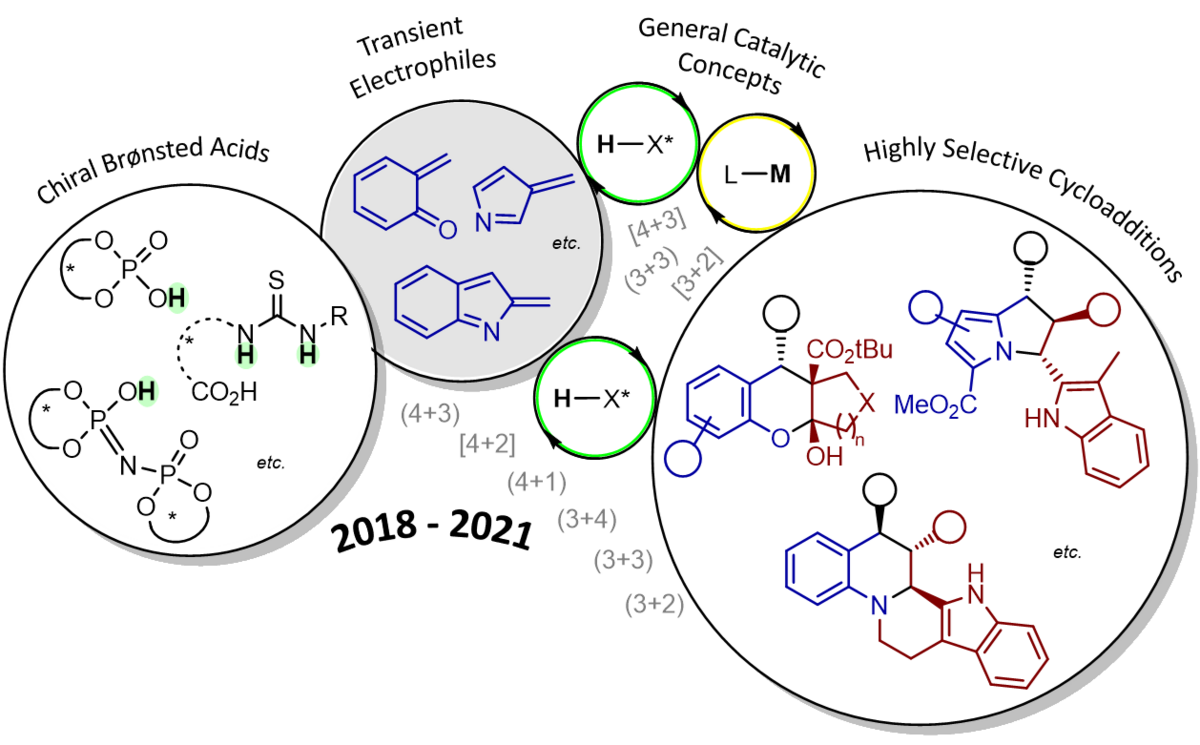
148. Asymmetrische Brønsted Säure-katalysierte Cycloadditionen von ortho-Chinonmethiden und verwandten Verbindungen (Übersichtsartikel)
C. Dorsch, C. Schneider
Inhalt: Dieser Übersichtsartikel fasst die Entwicklungen auf dem Gebiet der Brønsted-Säure katalysierten enantioselektiven Cycloaddition von ortho-Chinonmethiden, ortho-Chinonmethidiminen sowie heterocyclischen Indol- und Pyrrol-basierten Methidanaloga der letzten Jahre zusammen. Wertvolle polycyclische N- und O-Heterocyclen können in einem simplen Schritt ausgehend von einfachen Benzyl- und Heterobenzylalkoholen durch Dehydratisierung aufgebaut werden. Chirale Brønsted-Säuren formen Wasserstoffbrücken zu den transienten Reaktanden und können somit die Enantioselektivität der Prozesse gewährleisten. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Synthesis 2022, 54, 3125-3141. Publikation lesen
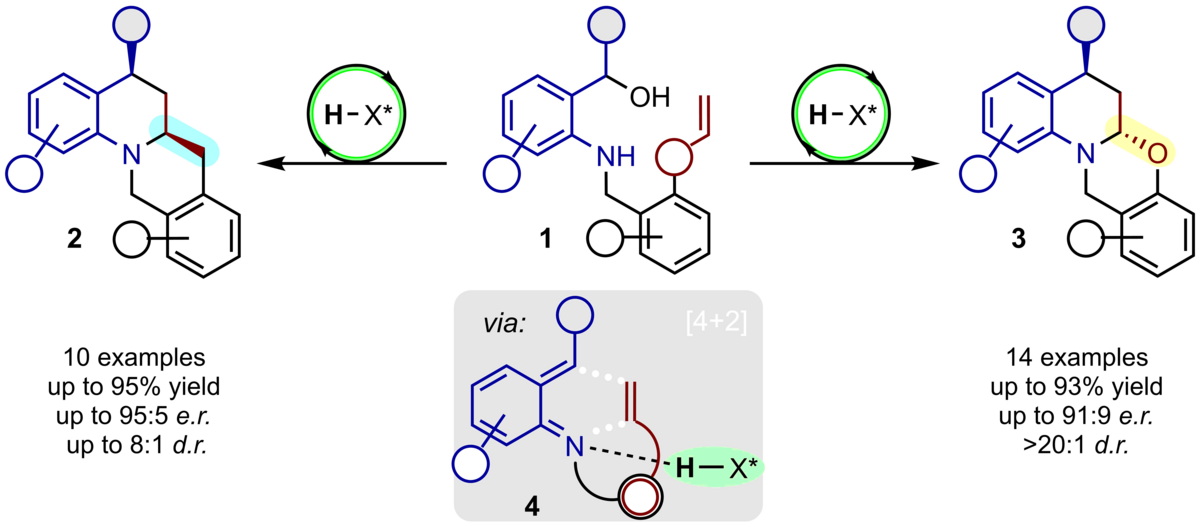
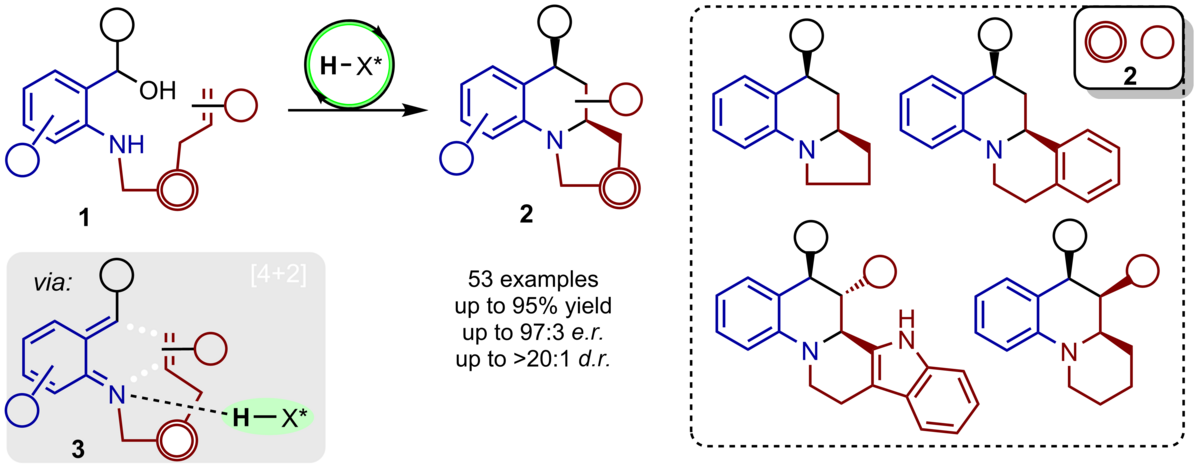
147. Intramolekulare Aza‐Diels‐Alder‐Reaktionen von ortho‐Chinonmethidiminen zu annellierten Tetrahydrochinolinen
F. Hofmann, C. Gärtner, M. Kretzschmar, C. Schneider
Inhalt: Aza-Diels-Alder-Reaktionen sind leistungsfähige Prozesse zum Aufbau von N-Heterocyclen und zeichnen sich durch ihre inhärente Atomökonomie und Stereospezifität aus. Intramolekulare Strategien erlauben die Bildung bicyclischer Strukturen mit bis zu drei Stereozentren in einem einzigen Schritt. Dieses Konzept wird mit der Chemie von Brønsted-Säure-aktivierten ortho-Chinonmethidiminen kombiniert, um eine umfangreiche Auswahl von interessanten anellierten Tetrahydrochinolinen auf diastereo- und enantioselektive Weise zu generieren. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Eingeladener Artikel im Rahmen des Special Topics zum siebzigjährigen Jubiläum der Verleihung des Nobelpreises an Otto Diels und Kurt Alder.
Synthesis 2022, 54, 1055-1080. Publikation lesen
146. Brønsted Säure-katalysierte (3+2)-Cycloaddition von Thioketonen und Indol-2-carbinolen zur Synthese von Thiazolo[3,4-a]indolen
F. Sachse, C. Schneider
Inhalt: Ein Brønsted-Säure katalysierter Ansatz erlaubte den Zugang zu den bislang unbekannten Thiazolo[3,4-a]indolen. Bei der (3+2)‑Cycloaddition zwischen stabilen Thioketonen und in situ erzeugten Indol‑2‑Methiden wurde eine große Bandbreite der Zielprodukte unter milden Bedingungen in Ausbeuten von 45-99 % erhalten. Die Praktikabilität des Prozesses und das synthetische Potenzial der Produkte wurden durch ein Upscaling‑Experiment und einige Folgetransformationen demonstriert. Zusätzlich konnten mithilfe diverser Kontrollexperimente mechanistische Einblicke in die Reaktion erhalten werden. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Adv. Synth. Catal. 2022, 364, 77-81. Publikation lesen
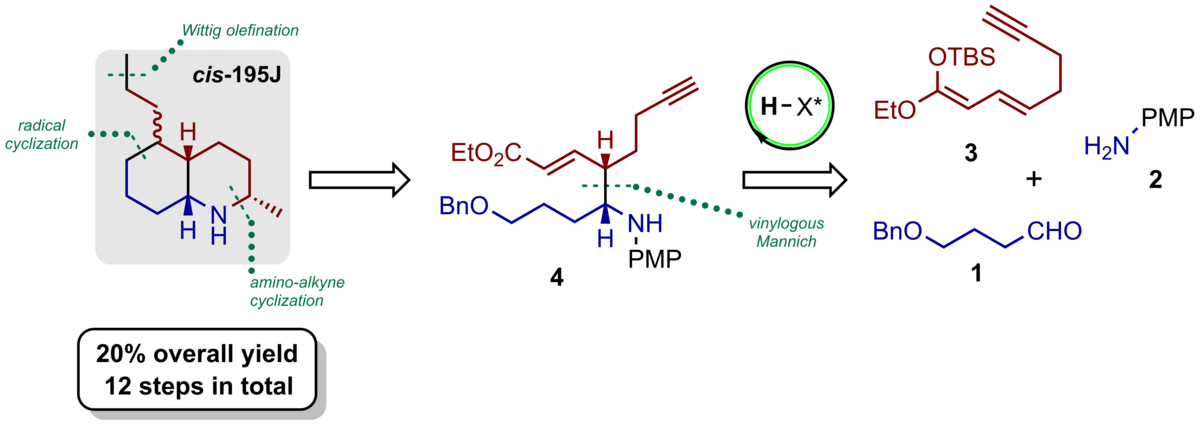
145. Stereoselektive Synthese des Decahydrochinolin-Alkaloids cis-195J
R. Veliu, C. Schneider
Inhalt: Zwei C-5-Diastereomere des Decahydrochinolin-Alkaloids cis-195J, dessen Struktur und Verknüpfung bis dato nicht verifiziert war, wurden erfolgreich enantioselektiv in 12 Schritten synthetisiert. Der Schlüsselschritt unserer Strategie ist die hochstereoselektive vinyloge Mukaiyama-Mannich-Reaktion (VMMR), welche die ersten beiden Stereozentren in 4 effzient etabliert und damit die Ringverknüpfung im Naturstoff definiert. Durch die Amin-Alkin-Cyclisierung und Enamin-Reduktion wurde die korrekte cis-Konfiguration zwischen C-2, C-4a und C-8a im Decahydrochinolin-Grundgerüst hergestellt. Anschließend wurde das bicyclische cis-Decahydrochinolin-Gerüst durch radikalische Cyclisierung eines Alkyliodids an den konjugierten Ester als Gemisch von zwei C-5-Diastereomeren aufgebaut. Weiterführende Modifikationen der C-5-Seitenkette lieferten schließlich beide Diastereomere von cis-195J, die sich leicht trennen ließen und deren Konstitution und Konfiguration erstmals eindeutig nachgewiesen werden konnten. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
J. Org. Chem 2021, 86, 11960–11967. Publikation lesen
Kommentiert: in "Alkaloid Synthesis" (D. F. Taber) 2022. KOMMENTAR Lesen
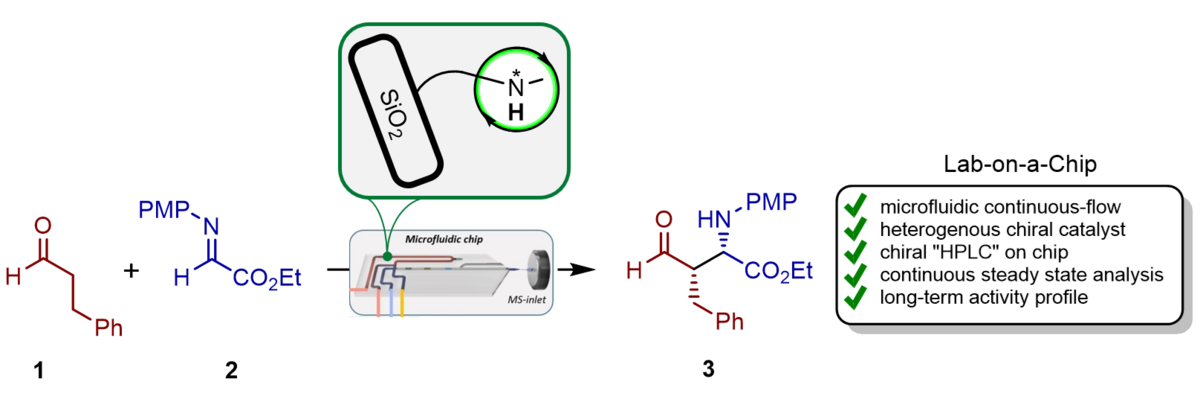
144. Direkter Einblick – Untersuchungen von immobilisierten Organokatalysatoren im Steady-State Betrieb durch Lab-on-Chip Technologie
H. Westphal, R. Warias, H. Becker, M. Spanka, D. Ragno, R. Gläser, C. Schneider, A. Massi, D. Belder
Inhalt: Eine neue Methode für die Untersuchung von stereoselektiven katalysierten Reaktionen im Kleinstmengenmaßstab wurde entwickelt. Dazu wurde ein miniaturisierter Festbettreaktor und eine chirale Chromatographiesäule auf einen Mikrodurchfluss-Chip kombiniert und direkt mit einem Massenspektrometer gekoppelt. Durch eine vollautomatisierte Injektionsstrategie konnten mit diesem Aufbau katalytische Prozesse und ihre Stereoselektivitäten im kontinuierlichen Durchflussverfahren über einen längeren Zeitraum verfolgt werden und wichtige Daten zur Degradierung bzw. Deaktivierung des im Reaktor integrierten chiralen heterogen-gebunden Organokatalysators gewonnen werden. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
ChemCatChem 2021, 13, 5089-5096. Publikation lesen
143. Kooperative Photo-induzierte-/Brønsted Säure-katalysierte Cycloaddition von in-situ erzeugten Thioaldehyden und ortho-Chinonmethiden zur Synthese von Benzo[e][1,3]oxathiinen
F. Sachse, C. Schneider
Inhalt: Eine thia‑Diels‑Alder Reaktion ermöglicht erstmalig den direkten Aufbau hochfunktionalisierter Benzo[e][1,3]benzooxathiane in guten bis exzellenten Ausbeuten und Diastereoselektivitäten aus zwei instabilen Intermediaten, einem Thioaldehyd und einem ortho‑Chinonmethid. Dabei wurden beide Reaktionspartner kooperativ und in-situ generiert. Im Prozess wurden sowohl elektronenreiche und elektronenarme Thioaldehyde als auch eine große Bandbreite von ortho‑Chinonmethiden problemlos toleriert, wodurch in kurzen Reaktionszeiten bei Raumtemperatur eine sehr große Vielfalt verschiedener S,O-Heterocyclen zugänglich gemacht werden konnte.(Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Org. Lett. 2021, 23, 2682–2686. Publikation lesen
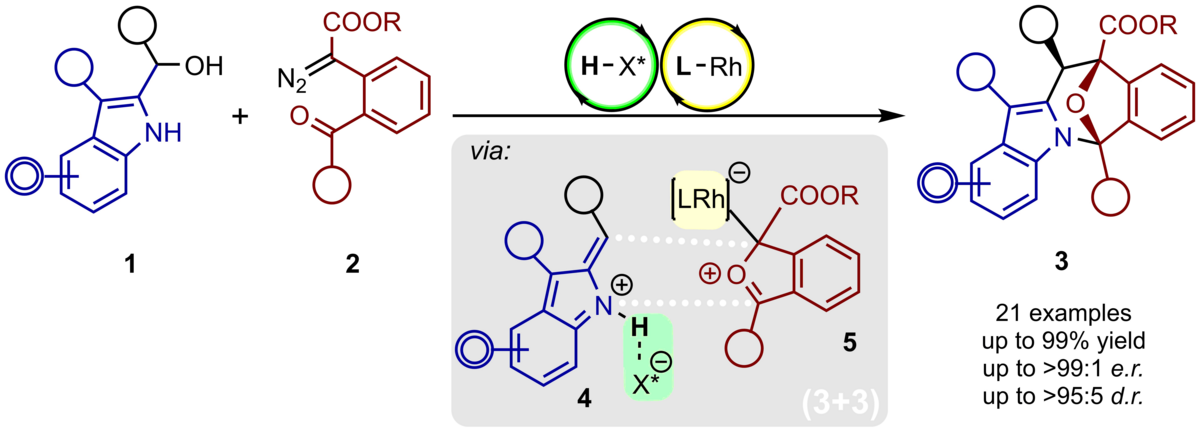
142. Hochstereoselektive (3+3)-Cycloanellierung von Carbonylyliden und Indolyl-2-methiden via kooperative Rh-/chirale Phosphorsäure-Katalyse
H. J. Loui, A. Suneja, C. Schneider
Inhalt: Die stereoselektiven (3+3)-Cycloanellierung von in-situ erzeugten Carbonylyliden mit Indolyl-2-methiden liefert sauerstoffverbrückte Azepino[1,2a]-indole in einem synthetischen Schritt. Der Prozess wird durch ein kooperatives Rh-/chirale Phosphorsäure-Katalysatorsystem ermöglicht, dass beide transienten Intermediate in voneinander unabhängigen Katalysecyclen erzeugt. Die Produkte wurden in guten bis exzellenten Ausbeuten erhalten, wobei ein tertiäres und zwei quartäre Stereozentren enantio- und diastereoselektiv aufgebaut werden konnten. In weiterführenden Transformationen konnten die Produkte zu wertvollen heterocyclischen Verbindungen umgesetzt werden. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Org. Lett. 2021, 23, 2578–2583. Publikation lesen
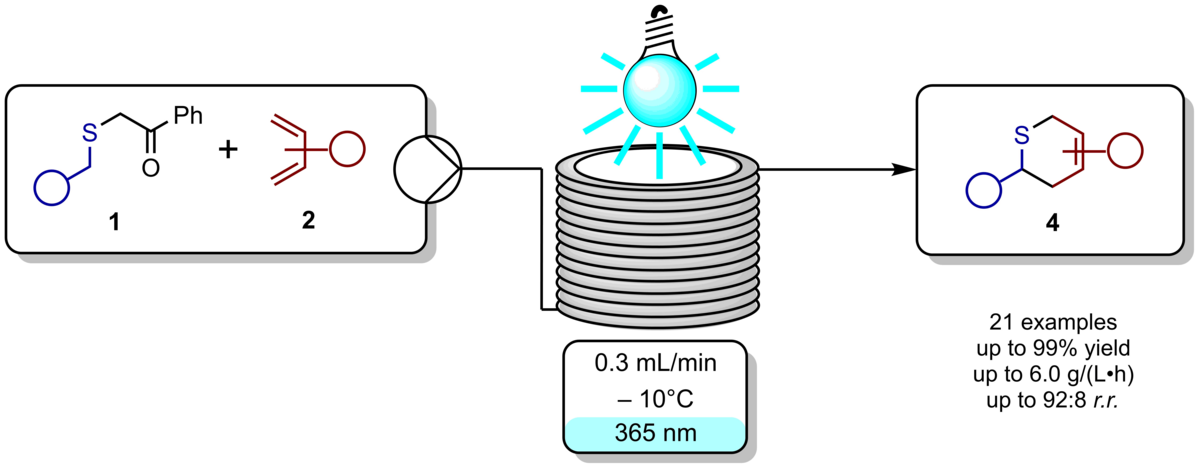
141. Synthese von 2H‑Thiopyranen im kontinuierlichen Durchflussverfahren via thia‐Diels‐Alder Reaktion von photochemisch erzeugten Thioaldehyden
F. Sachse, K. Gebauer, C. Schneider
Inhalt: Die photochemische Erzeugung und die direkte Weiterreaktion der hochreaktiven Thioaldehyde mit elektronen-reichen 1,3-Butadienen liefert im kontinuierlichen Durchflussverfahren die wertvollen Thia-Diels-Alder Produkte. Dabei konnte eine große Bandbreite an 3,6‐Dihydro‐2H‐thiopyranen in deutlich besseren Ausbeuten und Selektivitäten als in den vergleichbaren Batch-Verfahren synthetisiert werden. Stark reduzierte Reaktionszeiten und die Möglichkeit der nahtlosen Produktionserhöhung komplettieren die positive Bilanz des entwickelten Prozesses. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Eur. J. Org. Chem. 2021, 1, 64-71. Publikation lesen

Meine größte Motivation ist die Zusammenarbeit mit jungen, begeisterten Mitarbeitern … Meine wissenschaftlichen Lieblingsarbeiten sind die Publikationen von Woodward und Hoffmann zur Erhaltung der Orbitalsymmetrie ...
Christoph Schneider im Autoren-Profil
Dies und mehr von und über Christoph Schneider finden Sie in seinem Autoren‐Profil.
Angew. Chem. 2020, 132, 21462. publiKation LESEN
Angew. Chem. Int. Ed. 2020, 59, 21278. publiKation LESEN.
139. Brønsted-Säure-katalysierte (3+2)-Cycloanellierung von in-situ gebildeten 3-Methid-3H-pyrrolen: Asymmetrische Synthese von Cyclopenta[b]pyrrolen
I. Kallweit, M. Laue, C. Schneider
Inhalt: Eine organokatalysierte, hochenantioselektive Addition von cyclischen Enamiden 2 an in-situ gebildeten 3-Methid-3H-pyrrolen 4 liefert die polycylischen Cyclopenta[b]pyrrole 3 nach Cyclisierung und Eliminierung in exzellenten Enantioselektivitäten und sehr hohen Ausbeuten. Dabei ist der erfolgreiche Prozess eng mit der effizienten Maniplualtion der chiralen, Wasserstoffbrücken-gebundenen, hochreaktiven 3-Methid-3H-pyrrole 4 verknüpft, deren selektive Bildung über eine BINOL-Phosphorsäure (CPA)-katalysierten Dehydratisierung von 1H-Pyrrol-3-yl-carbinolen 1 erreicht wird. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Org. Lett. 2020, 22, 9065–9070. publiKation LESEN
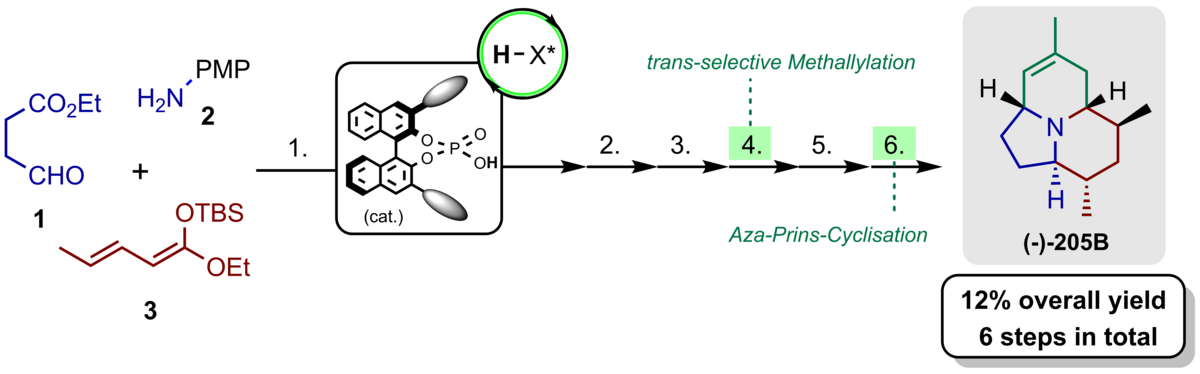
138. Eine kurze Synthese zum Alkaloid (-)-205B
M. Tripathy, C. Schneider
Inhalt: In nur 6 Schritten wurde das biologisch aktive Alkaloid (–)-205B in der eleganten, bis zu diesem Zeitpunkt kürzesten, stereoselektiven Synthese in einer Gesamtausbeute von 12% erhalten. Dabei ist die synthetische Herausforderung eng mit der tricyclischen Struktur und der darin enthaltenden fünf Stereozentren verknüpft. Die entwickelte Synthesesequenz zeichnet sich durch die Anwendung einer stereoselektiven, BINOL-Phosphorsäure (CPA)-katalysierten vinylogen Mannich-Reaktion, entwickelt in unserem Arbeitskreis, einer Zink-unterstützten Barbier-Methallylierung und einer Eintopf-Sequenz Lactam-Reduktion-Aza-Prins-Cyclisierung aus. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
J. Org. Chem. 2020, 85, 12724-12730. publiKation LEsen
Top 20: Unter den 20 meist-heruntergeladenen Publikationen des Journals J. Org. Chem. im Monat September 2020
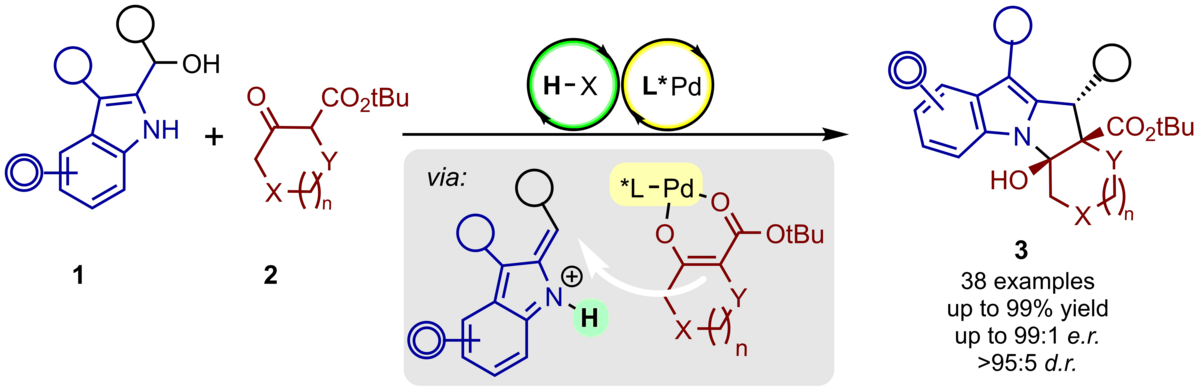
137. Palladium-katalysierte, enantioselektive (3+2)-Cycloanellierung von β-Keto Estern mit Alkyliden 2H-Indolen zur Synthese von komplexen Indol-basierten Heterocyclen
F. Göricke, C. Schneider
Inhalt: Die hochstereoselektive (3+2)-Cycloanellierung von chiralen Palladium-Enolaten mit vinylogen Iminiumionen, beide durch einen einzigen Palladium-Katalysator via duale Aktivierung in-situ gebildet, liefert hochfunktionalisierte Pyrrolo[1,2-a]indole in exzellenten Stereoselektivitäten (>95:5 d.r. und bis zu >99:1 e.r.) und Ausbeuten (bis zu 99%). Die Komplexität der Produkte wird durch die drei benachbarten Stereozentren und durch die synthetisch herausfordende tetracyclische Kernstrukur mit der [6–5–5–6] bzw. [6–5–5–5]-Verknüpfung charakterisiert. ESI-MS Studien und weitere Kontrollexperimente umreißen ein klares Bild des Reaktionsmechanismuses für den Schritt der Cycloannellierung. Ohne großen Aufwand können die Produkte modifiziert werden, um eine große Bandbreite an wertvollen, Indol-basierten und komplexen Heterocyclen zu erhalten. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Org. Lett. 2020, 22, 6101-6106. publiKation Lesen
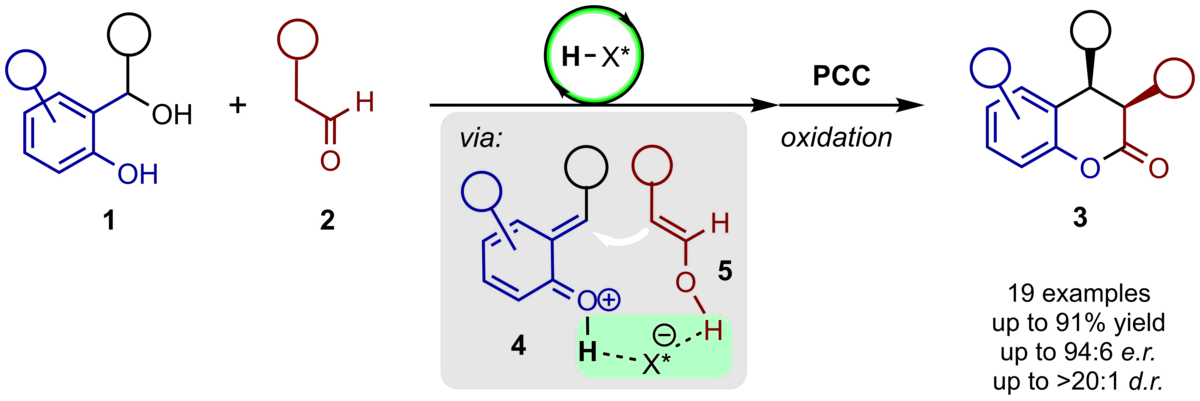
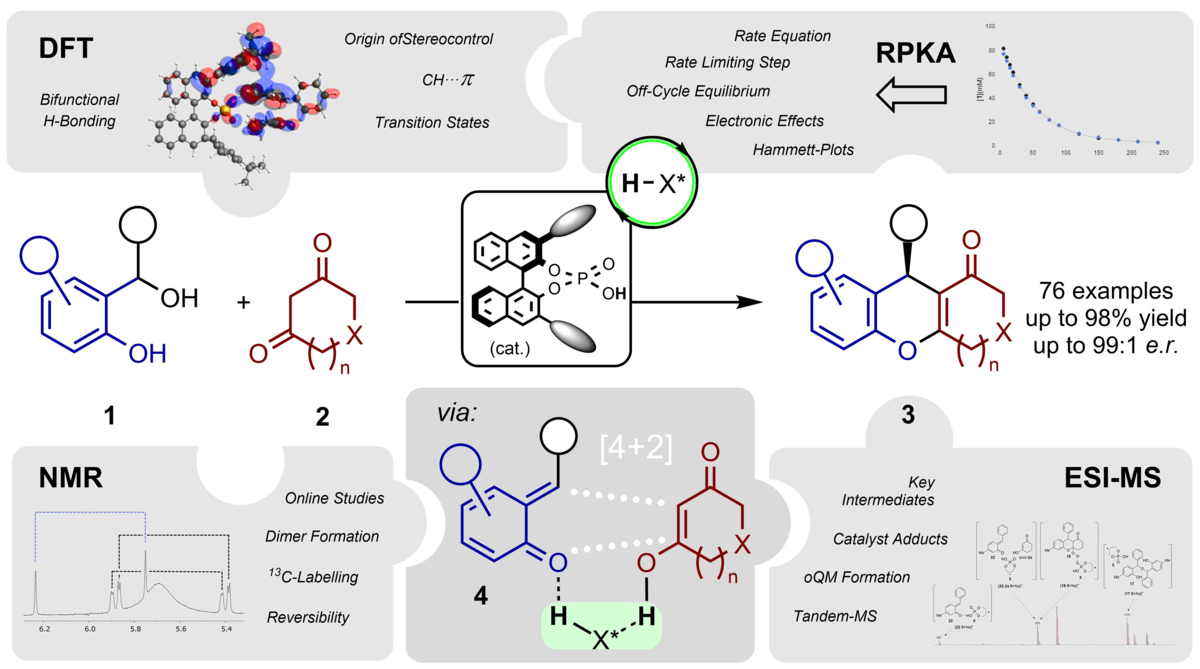
136. Phosphorsäure-katalysierte Bildung von Wasserstoffbrücken-gebundenen ortho-Chinonmethiden und deren enantioselektive Cycloaddition mit β-Dicarbonylen zur Synthese von benzanellierten, sauerstoffhaltigen Heterocyclen
F. Göricke, S. Haseloff, M. Laue, M. Schneider, T. Brumme, C. Schneider
Inhalt: Die BINOL-Phosphorsäure (H-X*)-katalysierte, enantioselektive Umsetzung von ortho-Hydroxybenzylalkoholen 1 mit β-Dicarbonylen 2 liefert 4H-Chromene und 1H-Xanthen-1-one 3 in exzellenten Ausbeuten und Enantioselektivitäten, wobei der zentrale Schritt durch die Brønsted Säure-katalysierte, enantioselektive Cycloaddition von β-Diketonen, β-Ketonitrilen und β-Ketoester an in-situ generierte, Wasserstoffbrücken-gebundene ortho-Chinonmethide 4 charakterisiert wird. Auf Grundlage von detaillierten mechanistischen Studien inklusive Online-NMR und ESI-MS Messungen sind Reaktionsintermediate und Reaktionspfade identifiziert worden, die einen klaren und tiefen Einblick in den Reaktionsmechanismus erlauben. Unteranderem ist ein Gleichwicht außerhalb des produktiven Katalysecylus verantwortlich, dass das hochreaktive ortho-Chinonmethid, über Dehydratisierung von ortho-Hydroxybenzylalkoholen in-situ erzeugt, auch mit schwachen Nucleophilen umgesetzt werden kann. In dem es zwischenzeitlich und reversible ein Addukt mit einem weiteren Molekül 1 bildet, wird ein Reservoir angelegt, aus welchem bei Bedarf das ortho-Chinonmethid für den produktiven Katalysecyclus regeniert wird. Kinetische Messungen erlaubten die Erstellungen von Reaktionsprofilen und die Bestimmung der Geschwindigkeitskonstanten und untermauerten, dass der geschwindigkeitsbestimmende Schritt die Bildung des ortho-Chinonmethide ist. Diese Studien zeigen zudem, dass die Stabilisierung der ortho-Chinonmethide durch die elektronischen Effekte der Substituenten und die Reaktionsgeschwindigkeit des beschriebenen Prozesses in direkter Beziehung und im Einklang mit den Hammett-Plots zueinanderstehen. DFT-Berechnungen bestätigen, dass eine konzertierte, aber höchst asynchron verlaufende [4+2]-Cycloaddition im Schlüsselschritt stattfindet und dass die Stereoinduktion durch attraktive CH−π Wechselwirkungen zwischen der am Katalysator befindlichen tBu-Gruppe und dem ortho-Chinonmethid begünstigt wird. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
J. Org. Chem. 2020, 85, 11699-11720. Publikation Lesen
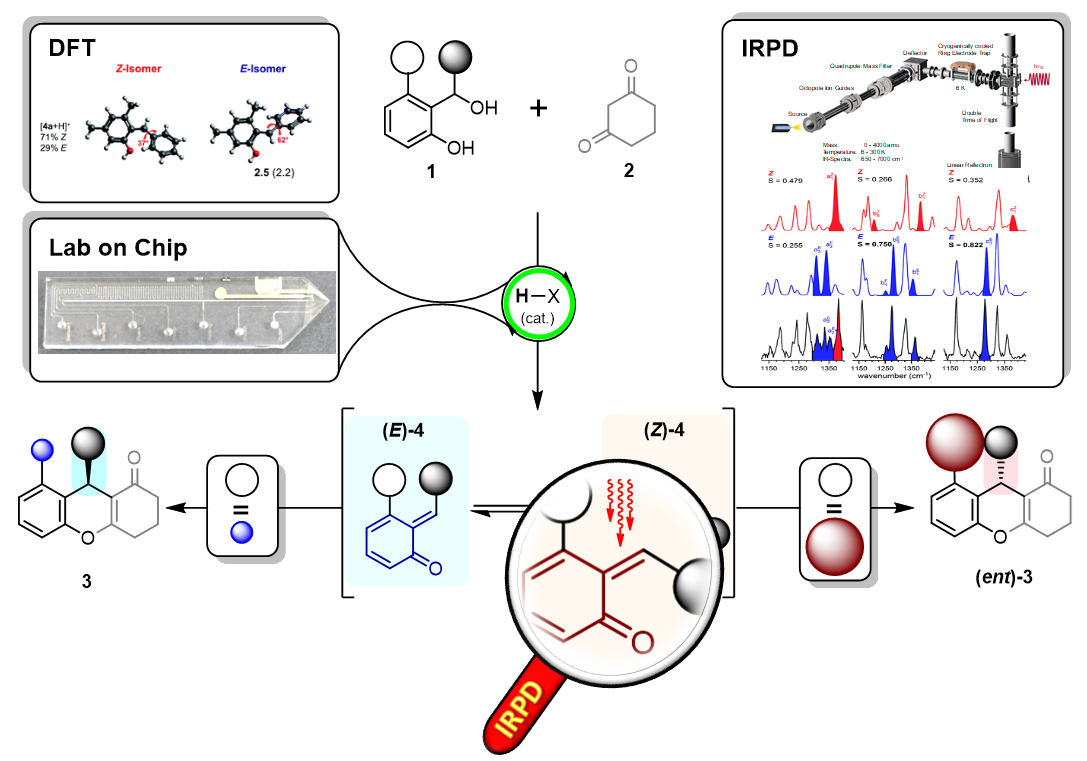
134. Rätsel gelöst: Bestimmung der Konfiguration der schnelllebigen und hochreaktiven ortho-Chinonmethide durch Kombination der Mikrofluid-Reaktortechnik mit Gasphasen-Schwingungsspektroskopie
M. Mayer, M. Pahl, M. Spanka, M. Grellmann, M. Sickert, C. Schneider, K. R. Asmis, D. Belder
Inhalt: Mit vereinten Kräften zur Lösung eines Rätsels: Die Konfiguration der Alkylidendoppelbindung der schnelllebigen ortho-Chinonmethide 4 ist mithilfe der kryogenen Ionenfallen-unterstützten Schwingungsspektroskopie untersucht worden. Zu diesem Zweck wurden die ortho-Chinonmethide 4 in einem mikrofluiden Chipreaktor in-situ über eine Brønsted-Säure (H-X) katalysierte Dehydratisierung von ortho-Hydroxybenzhydrylalkoholen 1 erzeugt und das E/Z-Isomerenverhältnis von 4 über Gasphasen-Infrarotspektroskopie im Fingerprintbereich bestimmt. Eine Zuordnung der Banden wurde durch den Vergleich mit Spektren, die über die DFT Berechnung erhalten wurden, realisiert. Zudem wurde gezeigt, dass sterische Wechselwirkungen zu einem in der Nähe befindlichen Substituenten, das Isomerenverhältnis von 4 und somit die chirale Induktion in asymmetrischen Additionsreaktionen mit Nucleophilen 2 direkt beeinflusst und damit experimentelle Befunde erklärt. Versuche, das Isomerenverhältnis durch Manipulation der Reaktionsbedingungen zu beeinflussen, waren nicht erfolgreich und unterstreichen, dass eine kleine Isomerierungsbarriere und damit eine schnelle Gleichgewichtseinstellung hinsichtlich der Verweilzeit auf dem Chip vorliegt. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Phys. Chem. Chem. Phys. 2020, 22, 4610-4616. Publikation Lesen
133. Kooperative Katalyse für die hochdiastereo- und enantioselektive (4+3)-Cycloanellierung von ortho-Chinonmethiden mit Carbonylyliden
A. Suneja, H. J. Loui, C. Schneider
Inhalt: Im Rahmen dieser Arbeit wurde ein Verfahren zur diastereo‐ und enantioselektiven (4+3)‐Cycloanellierung von ortho‐Chinonmethiden und Carbonylyliden entwickelt, das funktionalisierte, sauerstoffverbrückte Dibenzooxocine in exzellenten Ausbeuten und Stereoselektivitäten innerhalb eines einzelnen Syntheseschrittes zugänglich macht. Die kooperative Katalyse von Rhodium und einer chiralen Brønsted‐Säure (H-X*) ermöglicht die in-situ Erzeugung zweier hochreaktiver Intermediate, die zu komplexen, bicyclischen Produkten mit einem tertiären und zwei quartären Stereozentren reagieren. Diese wurden durch weitere Transformationen in wertvolle, enantiomerenangereicherte Synthesebausteine überführt. (Titel und Abstract basierend auf dem Originalartikel)
Angew. Chem. 2020, 132, 5580-5585. Publikation Lesen
Angew. Chem. Int. Ed. 2020, 59, 5536-5540. Publikation Lesen
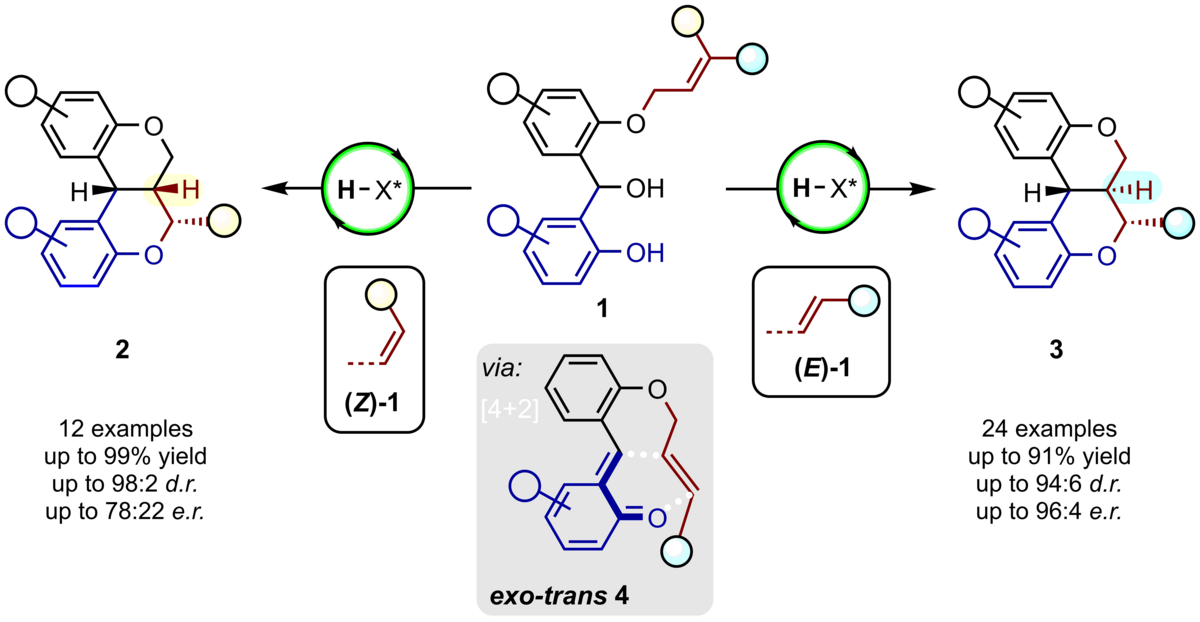
132. Brønsted Säure-katalysierte, diastereo- und enantioselektive, intramolekulare Oxa-Diels-Alder Reaktion von ortho-Chinonmethide und nicht-aktivierten Dienophilen
R. Ukis, C. Schneider
Inhalt: Eine stereoselektive, Phosphorsäure (H-X*)-katalysierte Synthese von Dihydrochromenchromenen 1 wurde von uns entwickelt und basiert auf der Verwendung der in-situ erzeugten schnelllebigen und hochreaktiven ortho-Chinonmethide 4. Drei stereogenen Zentren wurden dabei aufgebaut und die Produkte 2 und 3 in exzellenten Ausbeuten und Selektivitäten erhalten. Diese intramolekulare Hetero-Diels-Alder Reaktion wird durch die Verknüpfung von nicht-aktivierten Dienophilen an ortho-Chinonmethid-Vorläufer über einfache Phenoxy-Linker charakterisiert und erlaubt den Zugang zu Cycloaddukten, die als prominente Strukturmotive in einer Vielzahl von Naturstoffen wieder zufinden sind. Je nach Wunsch kann über die einstellbare Dienophil-Konfiguration ((Z)-1 oder (E)-1) entweder selektiv das endo-Produkt 2 oder das exo-Produkt 3 in Enantiomerenverhältnisse bis zu 96:4 gebildet werden. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
J. Org. Chem. 2019, 84, 7175-7188. Publikation Lesen
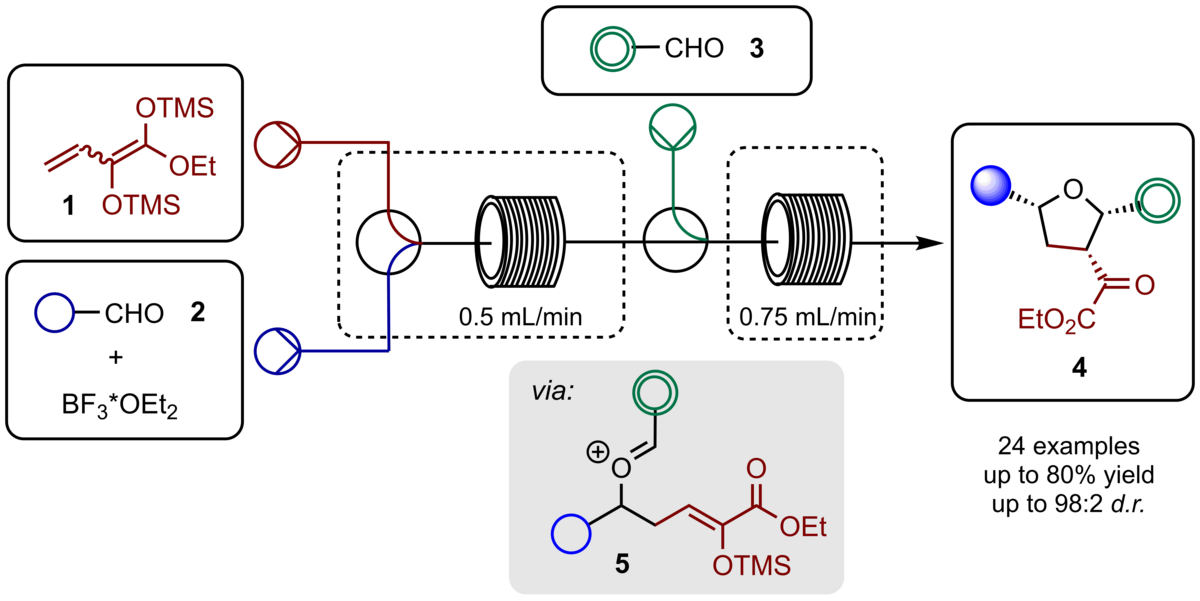
131. Synthese von hochsubstituierten Tetrahydrofuranen im kontinuierlichen Durchflussverfahren
P. Hoffmeyer, C. Schneider
Inhalt: Ein sequenzieller Prozess im kontinuierlichen Durchflussverfahren wurde von uns entwickelt zur hochdiastereoselektiven Synthese der hochsubstituierten Tetrahydrofurane 4. Deutlich reduzierte Reaktionszeiten, verbesserte Selektivitäten, Ausbeuten und Produktmengen im Multigramm-Maßstab wurden dabei als die wichtigsten Vorteile von diesem Verfahren gegenüber dem diskontinuierlichen Betrieb im Reaktionskolben identifiziert. Zusätzlich konnte der Zugang zu tetrasubstituierten Tetrahydrofuranen durch die Anwendung eines neuartigen Bis(silyl)diendiolates realisiert werden. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Eur. J. Org. Chem. 2019, 5326-5333. Publikation Lesen
Gewürdigt: in Synfacts 2019, 15, 0829. Publikation Lesen
Kommentiert: in "C-O Ring Construction" 2020. KOMMENTAR Lesen
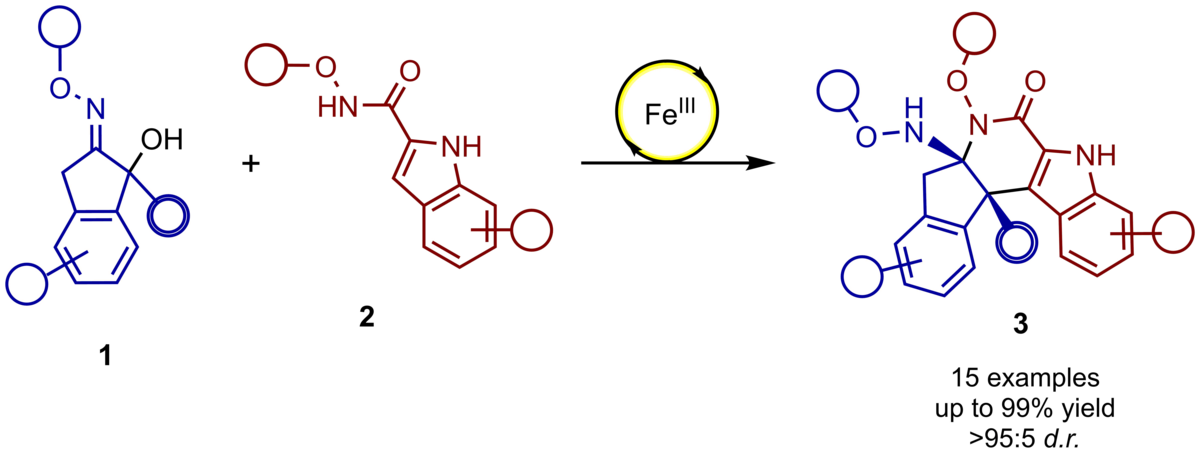
130. Eisen(III)-katalysierte (4+2)-Cycloanellierung von 2-Hydroxyketoximethern mit Indol-2ylamiden zur Synthese von Indol-verknüfpten 2-Piperidinonen
M. Schlegel, C. Schneider
Inhalt: Eine hochregio- und diastereoselektive (4+2)-Cycloanellierung von Indanon-abgeleiteten 2-Hydroxyketoximethern mit 1,4-bisnucleophilen Indol-2-ylamiden wurde von uns entwickelt. In der Gegenwart von katalytischen Mengen an FeCl3 konnten hochfunktionalsierte 2-Piperidinone isoliert werden, die entlang der zwei neuen Einfachbindungen zwei benachbarte quartäre Stereozentren aufweisen. Neben den milden Reaktionsbedingungen zeichnet sich diese Eintopf-Reaktion durch die sehr einfache Isolierung der Produkte per Filtration aus, wodurch der kostspielige und aufwendiger Aufreinigungsschritt der Säulenchromatographie vermieden werden konnte. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
J. Org. Chem. 2019, 84, 5886-5892. Publikation Lesen
129. Brønsted Säure-katalysierte [6+2]-Cycloaddition von 2-Vinylindoles mit in-situ generierten 2-Methid-2H-pyrrolen zur direkten, stereoselektiven Synthese von 2,3-Dihydro-1H-pyrrolizinen
I. Kallweit, C. Schneider
Inhalt: Eine organokatalysierte, diastereo- und enantioselektive (6+2)-Cycloaddition wurde von uns entwickelt zur Synthese von hochfunktionalsierten 2,3-Dihydro-1H-pyrrolizinen 3, die drei benachbarte Stereozentren aufweisen und deren prominente Kernstruktur in vielen biologisch aktiven Naturstoffen vertreten sind. Die Produkte 3 konnten in einem Schritt in guten Ausbeuten und exzellenten Enantioselektivitäten diastereomerenrein gewonnen werden. Die Grundlage für die exzellente Stereoselektivität bildet die Fähigkeit der BINOL-basierten chiralen Phosphorsäure (H-X*) beide Reaktanden 2 und 4 über ein Netzwerk aus Wasserstoffbrücken zu koordinieren, wobei zuvor der Katalysator über Dehydratisierung das hochreaktive 2-Methid-2H-pyrrol 4 aus dem 1H-Pyrrol-2ylcarbinol 1 generiert. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Org. Lett. 2019, 21, 519-523. Publikation Lesen
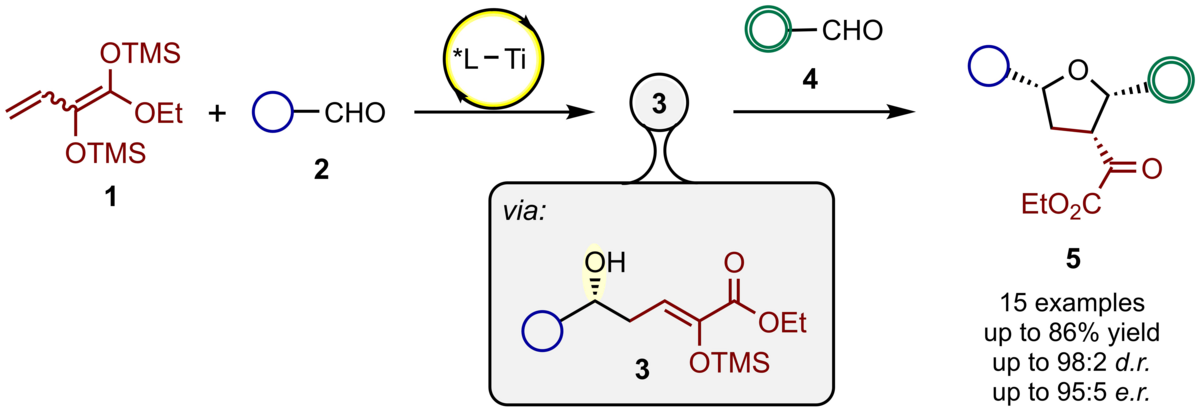
128. Stereoselektive Synthese von 2,3,5-trisubstituierten Tetrahydrofuranen eingeleitet durch eine Titan-BINOLat-katalysierte vinyloge Aldol Reaktion
P. Hoffmeyer, C. Schneider
Inhalt: Die enantioselektive Synthese von 2,3,5-trisubstituierten Tetrahydrofuranen 5 wurde von uns in einem sequenziellen Eintopf-Verfahren realisiert, bei der eine asymmetrische vinyloge Mukaiyama-Aldol Reaktion die Sequenz einleitet. In dieser mit einem Titan-BINOLat-Komplex (L*-TiIV) katalysierten Reaktion wird das Bis(silyl)diendiolat 1 mit dem Aldehyd 2 umgesetzt und das erste Stereozentrum im Zwischenprodukt 3 aufbaut. Im folgenden Schritt wird durch den Einsatz eines weiteren Aldehyds 4 und BF3*OEt2 die Prins-Cyclisierung von 3 zum Tetrahydrofuran 5 vollzogen und dabei im Allgemeinen gute Ausbeuten und gute bis sehr gute Enantio- und Diastereoselektivitäten beobachtet. In diesem Prozess werden insgesamt drei Bindungsknüpfungen realisiert und drei Stereozentren aufgebaut. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
J. Org. Chem. 2019, 84, 1079-1084. Publikation Lesen
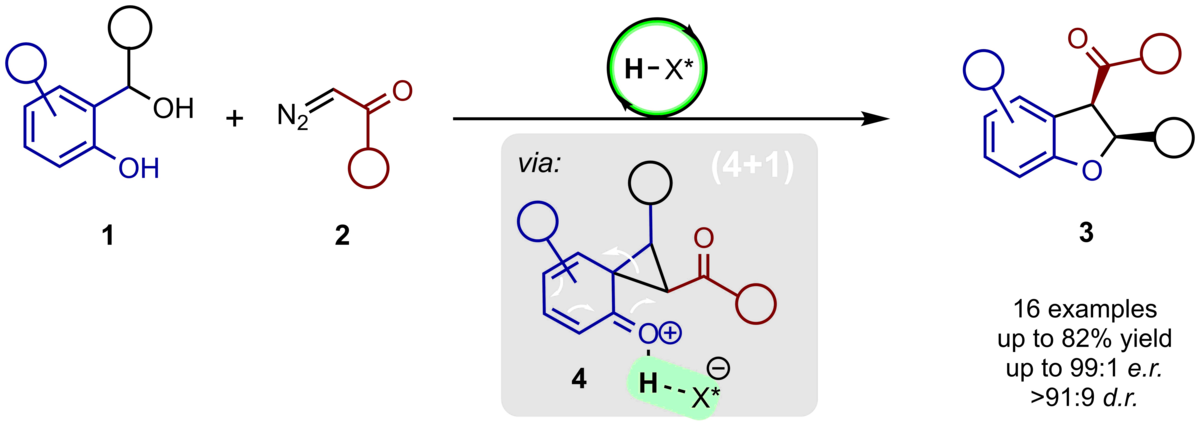
127. Brønsted Säure-katalysierte (4+1)-Cycloanellierung von ortho-Chinonmethiden und Diazoketonen
A. Suneja, C. Schneider
Inhalt: Eine direkte Route zu hochgradig enantiomerenangereicherten cis-2,3-Dihydrobenzofuranen 3 wurde von uns entwickelt, bei der Diazocarbonyle 2 in einer BINOL-Phosphorsäure (H-X*)-katalysierten (4+1)-Cycloanellierung an in-situ generierte ortho-Chinonmethide addieren. Die Produkte wurden in hohen Ausbeuten und sehr guten Diastereo- und Enantioselektivitäten. Das vorliegende invertierte 2,3-Verknüpfungsmuster in 3 kann anhand einer einzigartigen Phenonium-artigen Umlagerung über 4 erklärt werden. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Org. Lett. 2018, 20, 7576-7580. Publikation Lesen
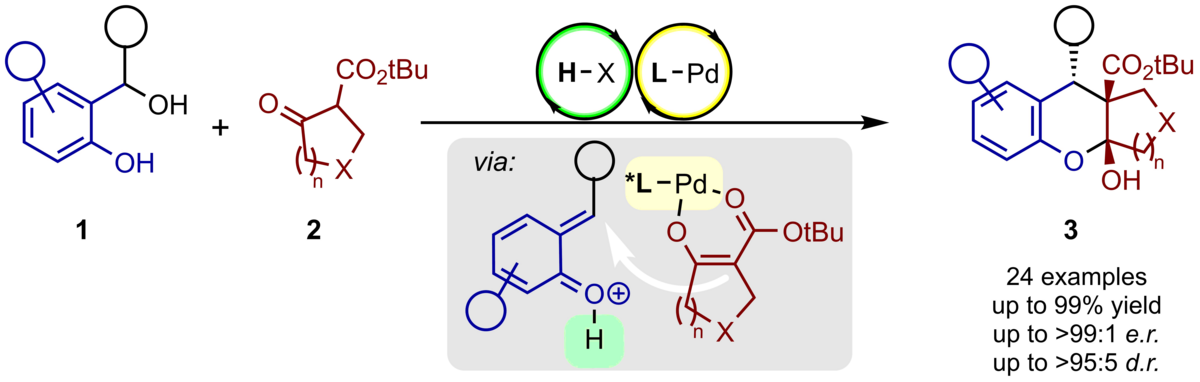
126. Palladium-katalysierte, enantioselektive Addition von chiralen Metall-Enolaten an in-situ generierte ortho-Chinonmethide
F. Göricke, C. Schneider
Inhalt: Chirale Palladium‐Aquakomplexe vermitteln die enantioselektive katalytische konjugierte Addition aus β‐Ketoestern 2 gebildeter chiraler Metallenolate an ortho‐Chinonmethide, die hochfunktionalisierte Chromane mit drei benachbarten Stereozentren hochstereoselektiv und in guten Ausbeuten liefert. Bei diesem Brønsted‐Säure/Base‐katalysierten kooperativen Prozess werden Nukleophil und Elektrophil durch einen chiralen Katalysator aktiviert. (Titel und Abstract basierend auf dem Originalartikel)
Angew. Chem. 2018, 130, 14952-14957. Publikation Lesen
Angew. Chem. Int. Ed. 2018, 57, 14736-14741. Publikation Lesen
Top 10%: Unter den 10% der meist-heruntergeladenen Publikationen des Journals Angew. Chem./Angew. Chem. Int. Ed. in den Monaten Dezember 2018 bis Januar 2019
Gewürdigt: in Synfacts 2019, 15, 0056. PUBLIKATION Lesen
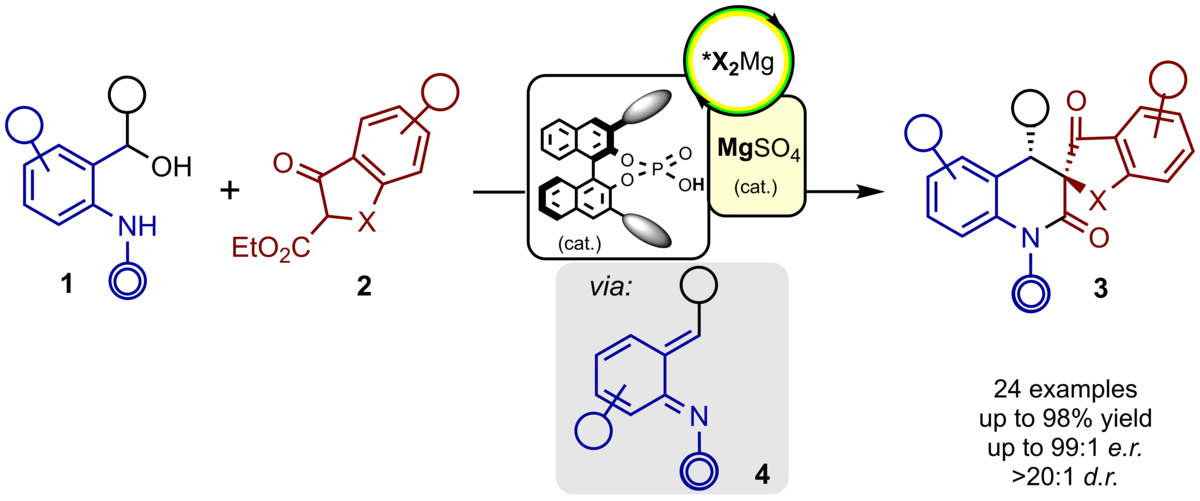
125. Eine hochenantio- und diastereoselektive Synthese von spirocyclischen Dihydrochinolinen via Domino-Michael-Addition-Lactamisierung von ortho-Chinonmethidiminen
T. Hodik, C. Schneider
Inhalt: Die Reaktion von in-situ erzeugten ortho-Chinonmethidiminen 4 mit cyclischen β‐Oxo Estern 2 lieferte spirocylische Dihydrochinoline 3 in guten Ausbeuten, mit exzellenter Diastereo- (> 20:1 d.r.) und Enantioselektivität (bis zu 99:1 e.r.). Dieser Domino-Prozess aus Michael Addition-Lactamisierung wird durch milde Reaktionsbedingungen, einfach zugängliche Startmaterialien und Produkte, die zwei neue und benachbarte Stereozentren aufweisen, charakterisiert. Mechanistische Untersuchungen untermauern, dass ein in-situ gebildeter chiraler Magnesium-Phosphat-Komplex eher für den Chiralitätstransfer und Reaktionsfortschritt verantwortlich ist als eine Katalyse durch die freie BINOL-Phosphorsäure (H-X*). (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Chem. Eur. J. 2018, 24, 18082-18088. Publikation Lesen
Top 10%: Unter den 10% der meist-heruntergeladenen Publikationen des Journals Chem. Eur. J. in den Monaten Dezember 2018 bis Januar 2019
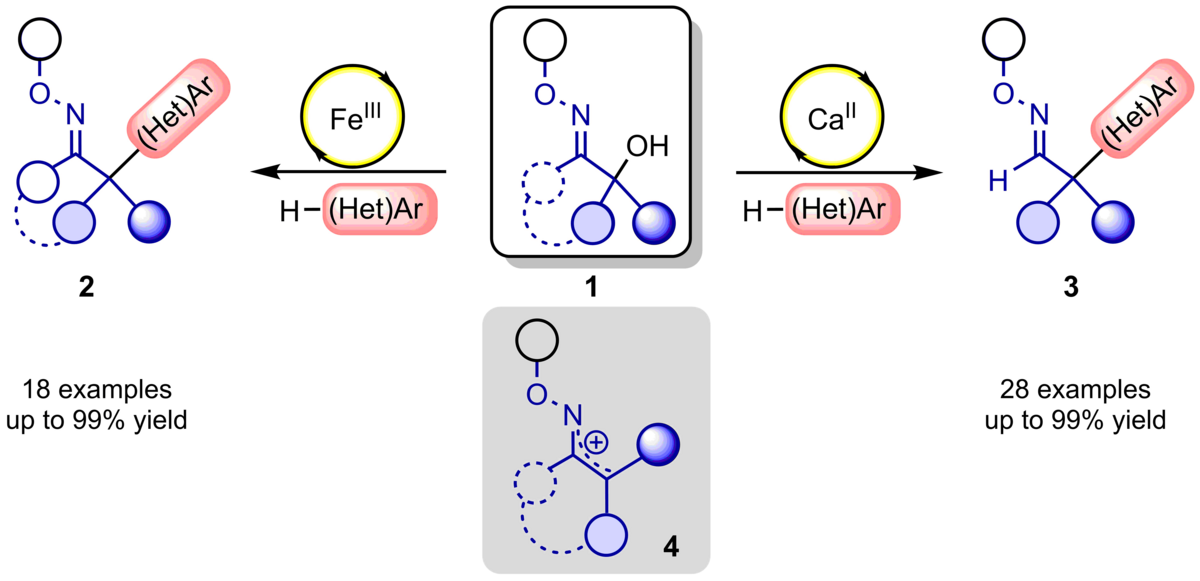
124. Lewis Säure-katalysierte Friedel-Crafts Reaktion zur Synthese von divers substituierbaren α-quartären Oximethern
M. Schlegel, C. Schneider
Inhalt: Die Synthese von komplett Kohlenstoff-substituierten, quartären Stereozentren durch Lewis Säure-katalysierte Alkylierung von cyclischen und acyclischen 2-Hydroxyloximethern 1 wurde von uns entwickelt. Die über Dehydratisierung von 1 in-situ gebildeten 1-Azaallylkationen 4 reagieren dabei unter milden Reaktionsbedingungen mit einer Reihe von elektronenreichen Aromaten und Heteroaromaten zu den Produkten 2 bzw. 3 in sehr guten Ausbeuten. Die auf diesem Weg erhaltenen Oximether 2 und 3 können anschließend sehr einfach in eine Vielzahl von weiteren funktionellen Gruppe transformiert werden. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Chem. Commun. 2018, 54, 11124-11127. Publikation Lesen
123. Phosphorsäure-katalysierte Addition von Aldehyden an in-situ generierte ortho-Chinonmethide - Ein enantio- und diastereoselektiver Zugang zu cis-Biaryl-dihydrocumarinen
M. Spanka, C. Schneider
Inhalt: Die stereoselektive, Phosphorsäure (H-X*)-katalysierte Synthese von cis-3,4-Diarylchromanolen wurde von uns entwickelt, bei der in-situ gebildete ortho-Chinonmethide 4 mit enolisierbaren Aldehyden 2 reagieren. Die hohe Stereoselektivität ist dabei eng mit der Fähigkeit des Katalysators (H-X*) verknüpft, im Schritt der chiralen Induktion über Wasserstoffbrücken beide reaktiven Intermediate 4 und 5 zu dirigieren und zuvor sowohl das ortho-Chinonmethid 4 über Dehydratisierung aus dem Hydroxylbenzyhdrylalkohol 1 als auch das Enol 5 aus dem Aldehyd 2 zu bilden. Im Anschluss können die cis-3,4-Diarylchromanole zu 3,4-Dihydrocumarinen 3, 4H-Chromenen und Chromanen in guten Gesamtausbeuten und mit sehr guten Diastereo- und Enantioselektivitäten überführt werden. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Org. Lett. 2018, 20, 4769-4762. Publikation Lesen
Gewürdigt: in Synfacts 2018, 14, 1090. PUBLIKATION Lesen
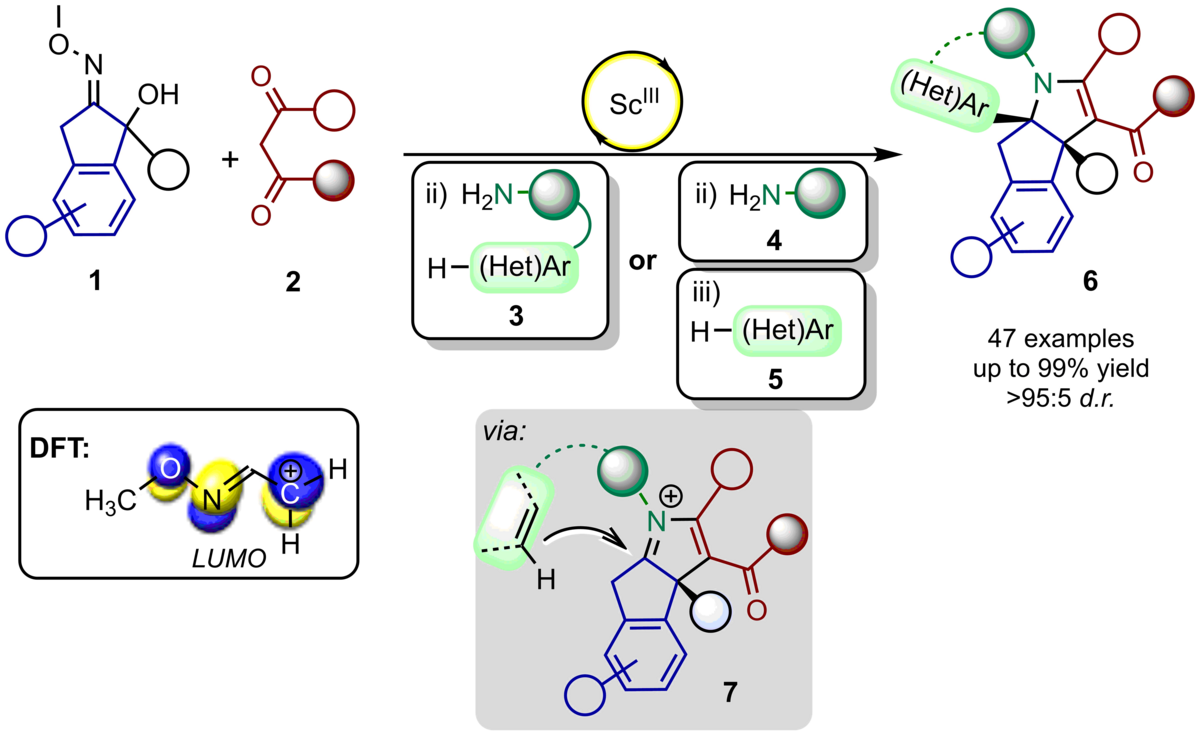
122. Eine neuartige, Scandiumtriflat-katalysierte (2+2+1)-Cycloanellierung/Aza-Friedel-Crafts Alkylierungssequenz zur Synthese von multicyclischen 2-Pyrrolinen
M. Schlegel, P. Coburger, C. Schneider
Inhalt: Der rasche und effiziente Aufbau von molekularer Komplexität ist ein gleichbleibendes und zugleich herausforderndes Ziel bei der Entwicklung von neuen Reaktionen. Im Zuge einer solchen Zielsetzung ist es uns gelungen, eine Scandiumtriflat-katalysierte Eintopf-Multikomponenten-Reaktion zu entwickeln, die den Zugang zu komplexen multicyclischen 2-Pyrrolinen im Einklang mit sehr hohen Gesamtausbeuten und perfekten Diastereoselektivitäten erlaubt. Dieser Prozess ist eine Weiterentwicklung der von uns kürzlich berichteten (2+2+1)-Cycloanellierung von in-situ generierten 1‐Azaallylkationen, welche durch Dehydratisierung von 1 erhalten werden, mit enolisierbaren 1,3-Dicarbonylen 2 und primären Aminen und bezieht seine Eleganz durch die Weiterfunktionalisierung der relativ labilen Aminalstruktur. Durch schlichtes Hinzufügen eines weiteren elektronenreichen Aromaten oder Heteroaromaten 4 bzw. eines mit π‐nucleophiler Gruppe funktionalisierten Amines 3 in der Eintopf-Sequenz können über das Iminiumkation 7 hochfunktionalisierte Stickstoffheterocylen erhalten werden, die zwei benachbarte quartäre Kohlenstoffe enthalten. Zusätzlich wurden im Rahmen dieser Arbeit die 1‐Azaallylkationen mittels DFT-Berechnungen näher untersucht und ihre Verwandtschaft in Reaktivität und Stabilisierung zu den gut-studierten Allylkationen bestätigt. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Chem. Eur J. 2018, 23, 14207-14212. Publikation Lesen
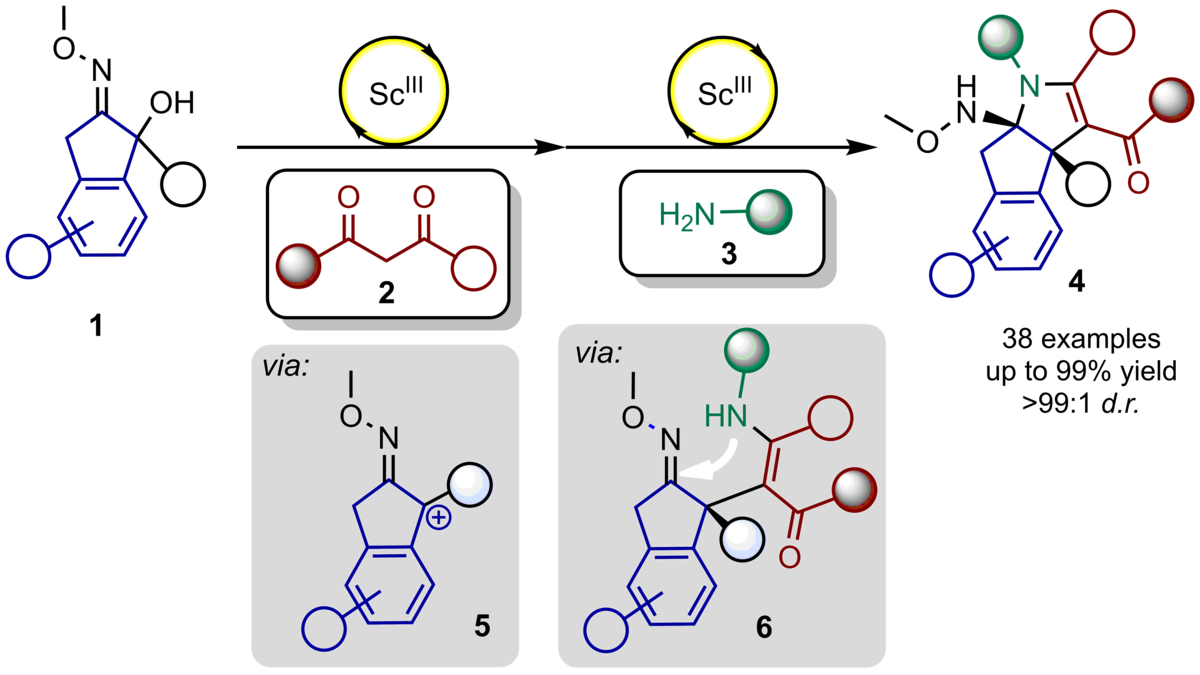
121. Ein schneller und effektiver Aufbau von komplex-strukturierten 2-Pyrrolinen durch Lewis Säure-katalysierte, sequenzielle Dreikomponenten Reaktion via in-situ generierte 1-Azaallylkationen
M. Schlegel, C. Schneider
Inhalt: Die erste Scandiumtriflat-katalysierte Dehydratisierung von 2-Hydroxyloximen 1 zur Erzeugung der hochreaktiven 1-Azaallylkationen 5 und deren Weiterreaktion mit enolisierbaren 1,3-Dicarbonylen 2 wurde von uns als sequenzielle Dreikomponenten-Reaktion entwickelt, bei der im letzten Schritt ein Amin 3 addiert wird. Diese (2+2+1)-Cycloanellierung erlaubt den Aufbau von vier neuen Einfachbindungen und zwei benachbarten quartären Stereozentren und liefert damit hochsubstituierte Tetrahydroindeno-[2,1-b]-pyrrole 4 in bis zu quantitativen Ausbeuten und perfekten Diastereoselektivitäten. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Org Lett. 2018, 20, 3119-3123. Publikation Lesen
120. Intramolekulare Aza‐Diels‐Alder‐Reaktionen von ortho‐Chinonmethidiminen – ein schneller, katalytischer und enantioselektiver Aufbau benzanellierter Chinolizidine
M. Kretzschmar, F. Hofmann, D. Moock, C. Schneider
Inhalt: Aza‐Diels‐Alder‐Reaktionen (ADARs) sind leistungsfähige Prozesse zum schnellen und stereoselektiven Aufbau von Stickstoffheterocyclen. Intramolekulare Varianten bieten darüber hinaus die Möglichkeit, bi‐ und polycyclische Ringsysteme in einem Schritt mit hoher Stereoselektivität zu generieren. In dem hier entwickelten Brønsted‐Säure (H-X*)‐katalysierten Verfahren können nun erstmals ortho‐Chinonmethidimine, die über den Iminsubstituenten an ein Dienophil gebunden sind, in einer enantioselektiven ADAR mit inversem Elektronenbedarf zu komplexen Chinolizidin‐ und Oxazinochinolin‐Ringsystemen umgesetzt werden. Die Reaktionen laufen unter milden Bedingungen in sehr guten Ausbeuten und mit guten bis sehr guten Diastereo‐ und Enantioselektivitäten ab. Das Verfahren kann darüber hinaus zu einem Domino‐Prozess erweitert werden, der Substratsynthese, ortho‐Chinonmethid‐Bildung und ADAR effizient vereinigt. (Titel und Abstract basierend auf dem Originalartikel)
Angew. Chem. 2018, 130, 4864-4868. Publikation Lesen
Angew. Chem. Int. Ed. 2018, 57, 4774-4778. Publikation Lesen
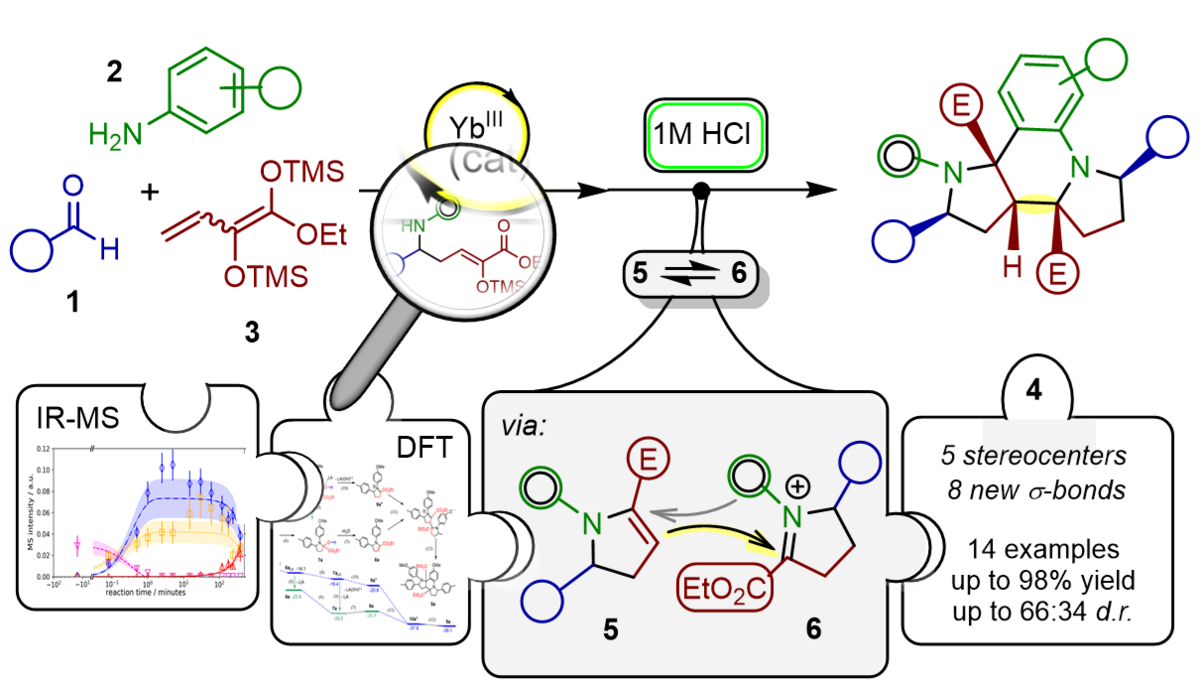
119. Modulare Synthese von Dipyrrolochinolinen - Eine Kombination aus synthetischer und mechanistischer Studie
J. Appun, F. Stolz, S. Naumov, B. Abel, C. Schneider
Inhalt: Eine direkte Synthese von [1,2-a][3′,2′-c]Dipyrrolochinolinen 4 wurde von uns entwickelt, bei der bis zu acht neue Bindungsknüpfungen und fünf neue Stereozentren in einer einfachen modularen Eintopf-Reaktion aufgebaut werden. Im Allgemeinen konnten die Produkte 4 in guten bis exzellenten Ausbeuten und mit moderaten bis guten Diastereoselektivitäten zugunsten der all-cis Konfiguration isoliert werden. Diese sequenzielle Transformation wird durch eine Lewis Säure-katalysierte, vinyloge Mukaiyama-Mannich Reaktion des Bis(silyl)diendiolates 3 eingeleitet, gefolgt von einer Brønsted Säure-unterstützten Mannich-Picted-Spengler Kaskaden-Reaktion (5+6), um das Dipyrrolochinolin als zentrales Strukturmotiv von 4 elegant und schnell aufzubauen. Neben ausführlichen synthetischen Untersuchungen wurde der Mechanismus der Reaktion anhand verschiedener analytischer Messverfahren (ESI- und Liquid-Beam IR-Laser Desorptionsmassensprektrometrie) begleitet von detaillierten DFT-Berechnungen aufgeschlüsselt. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
J. Org. Chem. 2018, 83, 1737-1744. Publikation Lesen
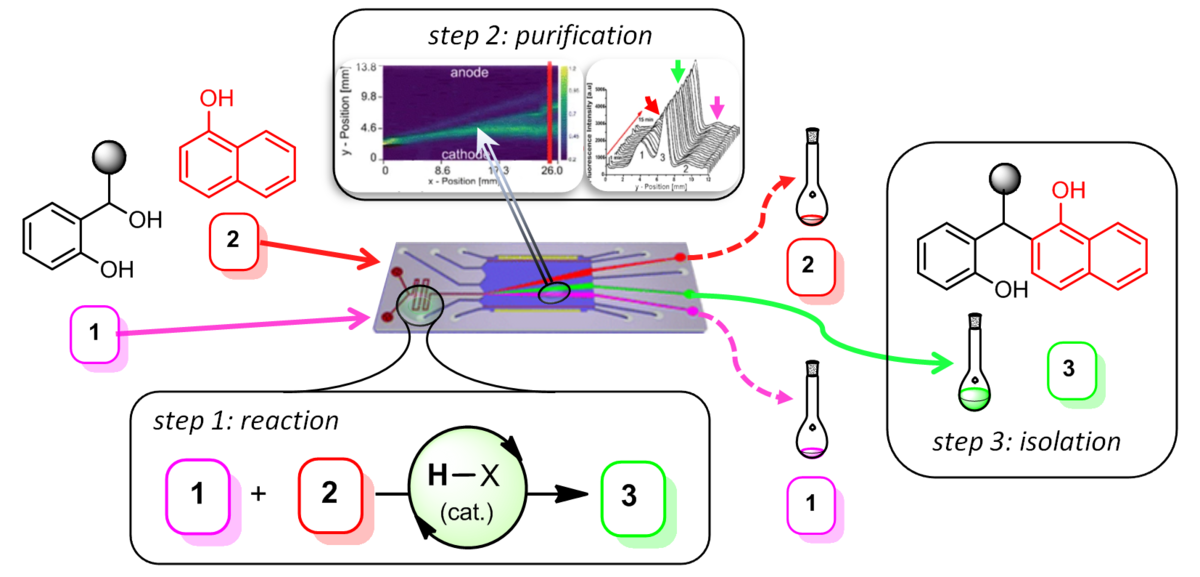
118. Kontinuierliche Reinigung von Reaktionsprodukten durch Mikro-Freifluß Elektrophorese mittels großflächiger Tiefen-UV Fluoreszenz Detektion
S. A. Pfeiffer, B. M. Rudisch, P. Glaeser, M. Spanka, F. Nitschke, A. A. Rubitzki, C. Schneider, S. Nagl, D. Belder
Inhalt: Eine Mikro-Freifluß Elektrophoreseeinheit wurde entwickelt, bei der Synthese, Reinigung und Isolierung auf einem Mikrochip vereint sind. Als Anwendungsbeispiel für den kontinuierlichen Betrieb wurde die säurekatalysierte Reaktion von Benzhydrylalkoholen 1 mit 1-Naphtholen 2 gewählt, die inklusive des Produktes 3 eine entsprechende on-line Detektion über Fluoreszenzextinktion gestatten. Für dieses Vorhaben wurde ein großflächiger Tiefen-UV Extinktionsfluoreszenz Detektionsbereich (3.6 cm²) im Setup des Chips integriert, um die Bedingungen für eine optimale Trennung der Reaktionspartner mittels Elektrophorese zu verifizieren. Im dritten Schritt konnten die Reaktionsprodukte und -partner isoliert werden und anhand Kapillarelektrophorese und Massenspektrometrie identifiziert werden. (Frei übersetzter Titel und Abstract basierend auf dem Originalartikel)
Anal. Bioanal. Chem. 2018, 410, 853-862. Publikation Lesen
- C. Schneider, M. Sickert
"The Mannich Reaction"
Science of Synthesis Knowledge Updates (M. Christmann, Ed.), Georg Thieme Verlag KG 2017/3, 315.
ISBN: 978-3-13-241419-8
DOI: 10.1055/sos-SD-140-00225
- K. Gebauer, F. Reuß, M. Spanka, C. Schneider
"Relay Catalysis: Manganese(III) Phosphate-Catalyzed Asymmetric Addition of β-Dicarbonyls to ortho-Quinone Methides Generated by Catalytic Aerobic Oxidation"
Org. Lett. 2017, 19, 4588-4591.
Highlighted in Synfacts 2018, 14, 63.
- J. Appun, M. Boomhoff, P. Hoffmeyer, I. Kallweit, M. Pahl, D. Belder, C. Schneider
"A New and Highly Stereoselective Synthesis of Tetrahydrofurans"
Angew. Chem. 2017, 129, 6862-6865.
Angew. Chem. Int. Ed. 2017, 56, 6758-6761.
Highlighted in CHEMIE.DE 2017.
Highlighted in Synfacts 2017, 13, 795.
Official press release of the University Leipzig, 14.06.2017, 141/2017.
- M. Schlegel, C. Schneider
"Lewis Acid-Catalyzed Nucleophilic Addition of Indoles to in situ-Generated 2-Amidoallyl Cations"
J. Org. Chem. 2017, 82, 5986-5992.
- S. Schulze, M. Pahl, F. Stolz, J. Appun, B. Abel, C. Schneider, D. Belder
"Liquid beam desorption mass spectrometry for the investigation of continuous flow reactions in microfluidic chips"
Anal. Chem. 2017, 89, 6175-6181.
- T. Hodik, C. Schneider
"Brønsted Acid-Catalyzed, Enantioselective Synthesis of 1,4-Dihydroquinoline-3-Carboxylates via In Situ Generated ortho-Quinone Methide Imines"
Org. Biomol. Chem. 2017, 15, 3706-3716.
- B. Abel, F. Stolz, J. Appun, S. Naumov, C. Schneider
"A complex catalytic reaction caught in the act: Intermediates and products online by liquid µ-beam mass spectrometry and theoretical modeling"
ChemPlusChem. 2017, 81, 233-240.
- C. Weilbeer, M. Sickert, S. Naumov, C. Schneider
"The Brønsted Acid-Catalyzed, Enantioselective Aza-Diels-Alder Reaction for the Direct Synthesis of Chiral Piperidones"
Chem. Eur. J. 2017, 23, 513-518.
- K. Gebauer, C. Schneider
"The First Organocatalytic Cope Rearrangement (Highlight)"
Angew. Chem. 2016, 128, 14416-14417.
Angew. Chem. Int. Ed. 2016, 55, 14208-14209.
- K. Bera, C. Schneider
"Brønsted Acid Catalyzed [3+2]-Cycloaddition of Cyclic Enamides with in Situ Generated 2-Methide-2H-indoles — Enantioselective Synthesis of Indolo[1,2-a]indoles"
Org. Lett. 2016, 18, 5660-5663.
- M. Kretzschmar, T. Hodik, C. Schneider
"Brønsted Acid Catalyzed Addition of Enamides to ortho-Quinone Methide Imines — An Efficient and Highly Enantioselective Synthesis of Chiral Tetrahydroacridines"
Angew. Chem. 2016, 128, 9941-9946.
Angew. Chem. Int. Ed. 2016, 55, 9788-9792.
Highlighted in Synfacts 2016, 12, 970.
- K. Bera, C. Schneider
"Brønsted Acid Catalyzed [3+2]-Cycloaddition of 2-Vinylindoles with In Situ Generated 2-Methide-2H-indoles — Highly Enantioselective Synthesis of Pyrrolo[1,2-a]indoles"
Chem. Eur. J. 2016, 22, 7074-7078.
- S. K. Alamsetti, M. Spanka, C. Schneider
"Synergistic Rhodium/Phosphoric Acid-Catalysis for the Enantioselective Additon of Oxonium Ylides to ortho-Quinone Methides"
Angew. Chem. 2016, 128, 2438-2442.
Angew. Chem. Int. Ed. 2016, 55, 2392-2396.
Highlighted in Synfacts 2016, 12, 376.
- V. A. Nikolaev, J. J. Medvedev, O. S. Galkina, K. V. Azarova, C. Schneider
"Unusual reactions of diazocarbonyl compounds with α,β-unsaturated δ-amino esters: Rh(II)-catalyzed Wolff rearrangement and oxidative cleavage of N–H-insertion products"
Beilstein J. Org. Chem 2016, 12, 1904-1910.
- C. Lindemann, C. Schneider
"Quinolizidine-Based Alkaloids – A General Catalytic, Highly Enantio- and Diastereoselective Synthetic Approach"
Synthesis 2016, 48, 828-844.
- P. R. Nareddy, C. Schneider
"A Highly Enantioselective, Organocatalytic [3+2]-Cycloannulation Reaction towards the de novo-Synthesis of 1-Cyclopentenyl-α-Keto Esters"
Chem. Commun. 2015, 51, 14797-14800.
Comment in "Organocatalyzed C-C Ring Construction" 2016.
- C. Dietze, T. Scholl, S. Ohla, J. Appun, C. Schneider, D. Belder
"Rapid prototyping of microfluidic chips for dead-volume-free MS coupling"
Anal. Bioanal. Chem. 2015, 29, 8735-8743.
- M. Boomhoff, R. Ukis, C. Schneider
"A Highly Stereocontrolled, One-Pot Approach towards Pyrrolobenzoxazinones and Pyrroloquinazolinones through a Lewis Acid-Catalyzed [3+2]-Cycloannulation Process"
J. Org. Chem. 2015, 80, 8236-8244.
- J. J. Medvedev, M. V. Meleshina, T. L. Panikorovskii, C. Schneider, V. A. Nikolaev
"Domino Reactions of Diazodicarbonyl Compounds with α,β-Unsaturated-δ-Amino Esters: Convenient Way Towards 2-Oxopiperidines, Dihydropyridinones, and Isoquinolinediones"
Org. Biomol. Chem. 2015, 13, 9107-9117.
- C. Benz, M. Boomhoff, J. Appun, C. Schneider, D. Belder
"Chip-Based Free-Flow Electrophoresis with Integrated Nanospray Mass-Spectrometry"
Angew. Chem. 2015, 127, 2805–2809.
Angew. Chem. Int. Ed. 2015, 54, 2766–2770.
- S. Saha, C. Schneider
"Directing Group Assisted Nucleophilic Substitution of Propargylic Alcohols via o-Quinone Methide Intermediates: Brønsted Acid Catalyzed, Highly Enantio- and Diastereoselective Synthesis of 7-Alkynyl-12a-acetamido-Substituted Benzoxanthenes"
Org. Lett. 2015, 17, 648–651.
- S. Saha, S. K. Alamsetti, C. Schneider
"Chiral Brønsted Acid-Catalyzed Friedel-Crafts Alkylation of Electron-Rich Arenes with in situ-Generated Ortho-Quinone Methides: Highly Enantioselective Synthesis of Diarylindolylmethanes and Triarylmethanes"
Chem. Commun 2015, 51, 1461–1464.
- S. Saha, C. Schneider
"Brønsted Acid-Catalyzed, Highly Enantioselective Addition of Enamides to in situ-Generated Ortho-Quinone Methides – A Domino Approach Towards the Direct Synthesis of Complex Acetamidotetrahydroxanthenes"
Chem. Eur J. 2015, 21, 2348–2352.
- J. J. Medvedev, O. S. Galkina, A. A. Klinkova, D. S. Giera, L. Hennig, C. Schneider, V. A. Nikolaev
"Domino [4 + 1]-annulation of α,β-unsaturated δ-amino esters with Rh(II)–carbenoids – a new approach towards multi-functionalized N-aryl pyrrolidines"
Org. Biolmol. Chem. 2015, 13, 2640–2651.
- M. Boomhoff, A. K. Yadav, J. Appun, C. Schneider
"Modular, Flexible, and Stereoselective Synthesis of Pyrroloquinolines – Rapid Assembly of Complex Heterocyclic Scaffolds"
Org. Lett. 2014, 16, 6236–6239.
- M. C. Pischl, C. F. Weise, S. Haseloff, M.-A. Müller, A. Pfaltz, C. Schneider
"A Highly Stereoselective and Flexible Strategy for the Convergent Synthesis of Long-Chain Polydeoxypropionates – Application towards the Synthesis of the Glycolipid Membrane Components Hydroxyphthioceranic and Phthioceranic Acid"
Chem. Eur. J. 2014, 20, 17360–17374.
- O. El-Sepelgy, S. Haseloff, S.K. Alamsetti, C. Schneider
"Brønsted Acid-Catalyzed, Conjugate Addition of β-Dicarbonyls to in situ Generated ortho-Quinone Methides – Enantioselective Synthesis of 4 Aryl-4H-Chromenes"
Angew. Chem. 2014, 126, 8057-8061.
Angew. Chem. Int. Ed. 2014, 53, 7923-7927.
Highlighted in Synfacts 2014, 10, 985.
- C. Schneider, F. Abels
"Catalytic, Enantioselective Vinylogous Michael Reactions" (Review)
Org. Biomol. Chem. 2014, 12, 3531-3543.
- F. Abels, C. Lindemann, C. Schneider
"A General Strategy for the Catalytic, Highly Enantio- and Diastereoselective Synthesis of Indolizidine-Based Alkaloids"
Chem. Eur. J. 2014, 20, 1964-1979.
- S. Basu, V. Gupta, J. Nickel, C. Schneider
"Organocatalytic Enantioselective Vinylogous Michael Reaction of Vinylketene Silyl-N,O-Acetals"
Org. Lett. 2014, 16, 274-277.
- C. Schneider, C. Weise
"Cope, Oxy-Cope, and Anionic Oxy-Cope Rearrangements"
Comprehensive Organic Synthesis 2nd Edition (G. Molander, P. Knochel, Eds.), Pergamon Press 2014, Vol. 5, 867-911.
- C. Schneider, M. Boomhoff
"Aldol Reactions in Domino Processes"
Domino Reactions - Concepts for Efficient Organic Synthesis, (L.F. Tietze, Ed.), Wiley-VCH 2014, 267-294.
- M. C. Pischl, C. F. Weise, M.-A. Müller, A. Pfaltz, C. Schneider
"A Convergent and Stereoselective Synthesis of the Glycolipid Components Phthioceranic Acid and Hydroxyphthioceranic Acid"
Angew. Chem. 2013, 125, 9138-9142.
Angew. Chem. Int. Ed. 2013, 52, 8968-8972.
- S. Peruncheralathan, S. Aurich, H. Teller, C. Schneider
"The Ti-BINOLate-Catalyzed, Enantioselective Ring-Opening of meso-Aziridines with Amines"
Org. Biomol. Chem. 2013, 11, 2787-2803.
- V. Gupta, S. Sudhir V., T. Mandal, C. Schneider
"Organocatalytic, Highly Enantioselective, Vinylogous Mukaiyama-Michael Reaction of Acyclic Dienolsilyl Ethers"
Angew. Chem. 2012, 124, 12778-12781.
Angew. Chem. Int. Ed. 2012, 51, 12609-12612.
Highlighted in Synfacts 2013, 9, 95.
Comment: www.organic-chemistry.org/Highlights/2013/08July.shtm
- F. Abels, C. Lindemann, E. Koch, C. Schneider
"A General Organocatalytic Approach toward the Enantioselective Total Synthesis of Indolizidine Based Alkaloids"
Org. Lett. 2012, 14, 5972-5975.
Comment: www.organic-chemistry.org/Highlights/2013/22April.shtm
- M. Boomhoff, C. Schneider
"A Novel 3-Component [3+2]-Cycloannulation Process for the Rapid and Highly Stereoselective Synthesis of Pyrrolobenzoxazoles"
Chem. Eur. J. 2012, 18, 4185-4189.
Highlighted in Synfacts 2012, 8, 606.
- C. F. Weise, M. Pischl, A. Pfaltz, C. Schneider
"A General, Asymmetric, and Non-Iterative Synthesis of Trideoxypropionates. Straightforward Syntheses of the Pheromones (+)-Vittatalactone and (+)-Norvittatalactone"
J. Org. Chem. 2012, 77, 1477-1488.
- A. Marti, S. Peruncheralathan, C. Schneider
„Cationic Late Transition Metal Complexes Catalyze the Ring-Opening of meso-Aziridines with Amines”
Synthesis 2012, 44, 27-36.
- C. F. Weise, F. Richter, S. Immel, C. Schneider
„The Oxy-Cope Rearrangement of Aldol Products - A Combined Experimental and Theoretical Study”
Eur. J. Org. Chem. 2012, 1520-1529.
- S. Ohla, R. Beyreiss, S. Fritzsche, P. Gläser, S. Nagl, K. Stockhausen, C. Schneider, D. Belder
„Monitoring on-Chip Pictet-Spengler Reaction by Integrated Analytical Separation and Label-Free Time-Resolved Fluorescence”
Chem. Eur. J. 2012, 18, 1240-1246.
- F. Abels, C. Schneider
„A Modified and Highly Useful Protocol for the Bronsted Acid-Catalyzed, Enantioselective, Vinylogous Mannich Reaction with Aliphatic Aldimines”
Synthesis 2011, 4050-4058.
Comment: www.organic-chemistry.org/Highlights/2012/30July.shtm
- S. Fritzsche, S. Ohla, P. Gläser, D. S. Giera, M. Sickert, C. Schneider, D. Belder
„Asymmetrische Organokatalyse und Analyse in einem mikrofluidschen Nanospray-Chip”
Angew. Chem. 2011, 123, 9639-9642.
Angew. Chem. Int. Ed. 2011, 50, 9467-9470.
Highlighted in Chem. Unserer Zeit 2011, 45, 370.
- B. M. Ruff, S. Zhong, M. Nieger, M. Sickert, C. Schneider, S. Bräse
„A. Combined Asymmetric Vinylogous Mannich/Diels-Alder Approach for the Stereoselective Synthesis of Highly Functionalized Hexahydroindoles”
Eur. J. Org. Chem. 2011, 6558-6566.
- A. Marti, L. Richter, C. Schneider
„Iron-Catalyzed Ring-Opening of meso-Aziridines with Amines”
Synlett 2011, 2513-2516.
Abstract: www.organic-chemistry.org/abstracts/lit3/426.shtm
- C. F. Weise, M. Pischl, A. Pfaltz, C. Schneider
„A Non-Iterative, Flexible, and Highly Stereoselective Synthesis of Polydeoxypropionates – Synthesis of Vittatalactone”
Chem. Commun. 2011, 47, 3248-3250.
- D. S. Giera, C. Schneider
"InCl3-Catalyzed Allylic Friedel-Crafts Reactions towards the Stereocontrolled Synthesis of 1,2,3,4-Tetrahydroquinolines"
Org. Lett. 2010, 12, 4884.
- H. Schönherr, J. Mollitor, C. Schneider
"A Chemoenzymatic Approach to the Stereocontrolled Synthesis of the C1-C11-Fragment of (+)-Peloruside A"
Eur. J. Org. Chem. 2010, 3908.
- C. Schneider, M. Sickert
"Catalytic, Enantioselective Vinylogous Mannich Reactions in Chiral Amine Synthesis, Methods, Developments and Applications (T. Nugent, Ed.)"
Wiley-VCH, Weinheim 2010, 157.
- M. Sickert, F. Abels, M. Lang, J. Sieler, C. Birkemeyer, C. Schneider
"The Brønsted Acid-Catalyzed, Enantioselective Vinylogous Mannich Reaction"
Chem. Eur. J. 2010, 16, 2806.
- S. Ghosh, M. V. Nandakumar, H. Krautscheid, C. Schneider
"Copper-Bipyridine-Catalyzed Enantioselective a-Amination of ß-Keto Esters"
Tetrahedron Lett. 2010, 51, 1860.
- M. V. Nandakumar, S. Ghosh, C. Schneider
"Enantioselective Synthesis of a Novel Chiral 2,9-Disubstituted 1,10-Phenanthroline and First Applications in Asymmetric Catalysis"
Eur. J. Org. Chem. 2009, 6393.
- C. Enkisch, C. Schneider
"Sequential Mannich-aza-Michael Reaction for the Stereodivergent Synthesis of Highly Substituted Pyrrolidines"
Eur. J. Org. Chem. 2009, 5549.
- D. S. Giera, M. Sickert, C. Schneider
"A Straightforward Synthesis of (-)-Anabasine through the Catalytic, Enantioselective, Vinylogous Mannich Reaction"
Synthesis 2009, 3797.
- S. Peruncheralathan, H. Teller, C.Schneider
"Ti-BINOLat-katalysierte Aminolyse von meso-Aziridinen - ein hochenantioselektiver und direkter Zugang zu 1,2-Diaminen"
Angew. Chem. 2009, 121, 4943.
Angew. Chem. Int. Ed. 2009, 48, 4849.
Highlighted in Synfacts 2009, 873.
- C. Schneider
"Katalytische, enantioselektive Ringöffnungen von Aziridinen"
Angew. Chem. 2009, 121, 2116.
Angew. Chem. Int. Ed. 2009, 48, 2082.
- D. S. Giera, M. Sickert, C. Schneider
"Brønsted Acid-Catalyzed, Enantioselective, Vinylogous Mannich Reaction of Vinylketene Silyl N,O-Acetals"
Org. Lett. 2008, 10, 4259.
- S. Khaliel, M. V. Nandakumar, H. Krautscheid, C. Schneider
"Organocatalytic Domino Mannich Aza-Michael Reactions towards the Stereoselective Synthesis of Highly Substituted Pipecolic Esters"
Synlett 2008, 2705.
- E. Mai, C. Schneider
"Catalytic, enantioselective synthesis of Boc-protected 1,2-amino alcohols through aminolysis of meso-epoxides with benzophenone imine"
Arkivoc 2008, 9, 216.
- M. Sickert, C. Schneider
"Enantioselektive, Brønstedt-Säure-katalysierte, vinyloge Mannich-Reaktion"
Angew. Chem. 2008, 120, 3687.
Angew. Chem. Int. Ed. 2008, 47, 3631.
Highlighted in Synfacts 2008, 756.
- A. Tschöp, M. V. Nandakumar, O. Pavlyuk, C. Schneider
"Scandium-Bipyridine-Catalyzed Selenol Addition to Aromatic meso-Epoxides"
Tetrahedron Lett. 2008, 49, 1030.
- S. Peruncheralathan, M. Henze, C. Schneider
"Indium(III) Chloride-Catalyzed Thiolysis of meso-Aziridines"
Tetrahedron Lett. 2007, 48, 6743.
- S. Peruncheralathan, M. Henze, C. Schneider
"Sc(OTf)3-Catalyzed Aminolysis of meso-Aziridines"
Synlett 2007, 2289.
- E. Mai, C. Schneider
"Indium-Bipyridine-Catalyzed, Enantioselective Aminolysis of meso-Epoxides"
Synlett 2007, 2136.
- M.V.Nandakumar, A. Tschöp, H. Krautscheid, C. Schneider
"Indium-Bipyridine-Catalyzed, Enantioselective Thiolysis of meso-Epoxides"
Chem. Commun. 2007, 2756.
Highlighted in Synfacts 2007, 960.
- F. Jakob, C. Schneider
"Enzyme-Catalyzed Kinetic Resolution of 1,3-Anti-Diol Monoesters. Efficient Preparation of Enantiomerically Highly Enriched and Unsymmetrically Substituted 1,3-Anti-Diols"
Eur. J. Org. Chem. 2007, 2958.
- A. Tschöp, A. Marx, A.R. Sreekanth, C. Schneider
"Scandium-Bipyridine-Catalyzed, Enantioselective Alcoholysis of meso-Epoxides"
Eur. J. Org. Chem. 2007, 2318.
- N. Remme, K. Koschek, C. Schneider
"Scandium-Triflate-Catalyzed Transesterification of Carboxylic Esters"
Synlett 2007, 491.
- E. Mai, C. Schneider
"The Scandium-Bipyridine-Catalyzed, Enantioselective Aminolysis of Meso-Epoxides"
Chem. Eur. J. 2007, 13, 2729.
- C. Schneider
"Synthesis of 1.2-Difunctionalized Fine Chemicals through Catalytic, Enantioselective Ring-Opening Reactions of Epoxides"
Synthesis 2006, 3919.
- C. Schneider, M. Hansch, P. Sreekumar
"Zirconium-BINOLate-catalyzed enantioselective aldol-Tishchenko reactions of aromatic ketone aldols"
Tetrahedron: Asymm. 2006, 17, 2738.
- C. Schneider, S. Khaliel
"Microwave-Assisted Silyloxy-Cope Rearrangements of syn-Aldol Products in DMF: Enhancement of Rate and Diastereoselectivity"
Synlett 2006, 1413.
- C. Schneider
"1,1-Bis(organooxy)alk-1-enes"
Science of Synthesis, Thieme, Vol. 24.2.6., 2006, 293.
- C. Schneider, M. Hansch
"The Zr(OtBu)4-Catalyzed Aldol-Tishchenko Reaction of Ketone Aldol Adducts"
Chem. Eur. J. 2005, 11, 3010.
- C. Schneider, K. Klapa, M. Hansch
"Zr(OtBu)4-Catalyzed Tishchenko Reduction of b-Hydroxy Ketones"
Synlett 2005, 91.
- C. Schneider, A. R. Sreekanth, E. Mai
"Scandium-Bipyridine-Catalyzed, Enantioselective Addition of Alcohols and Amines Towards meso-Epoxides"
Angew. Chem. 2004, 116, 5809-5812; Angew. Chem. Int. Ed. 2004, 43, 5691-5694.
- C. Schneider, M. Hansch
"First Catalytic, Enantioselective Aldol-Tishchenko Reactions with Ketone Aldol Adducts as Enol Equivalents"
Synlett 2003, 837.
- C. Schneider, F. Tolksdorf, M. Rehfeuter
"Asymmetric Synthesis of the Polyol Fragment of the Polyene Macrolide Antibiotic RK-397"
Synlett 2002, 2098.
- C. Schneider
"Katalytische, enantioselektive Synthesen von b-Lactonen - vielseitige Synthesebausteine in der Organischen Chemie (Highlight)" Angew. Chem., 2002, 114, 771; Angew. Chem. Int. Ed. 2002, 41, 744.
- C. Schneider
"Erste de novo-Synthese des Bisindolalkaloids Vinblastin (Highlight)"
Angew. Chem. 2002, 114, 4391; Angew. Chem. Int. Ed. 2002, 41, 4217.
- C. Schneider, O. Reese
"Highly Stereoselective and Efficient Synthesis of Functionalized Cyclohexanes with Multiple Stereocenters"
Chem. Eur. J. 2002, 8, 2585.
- C. Schneider, J. Brauner
"Lewis Base Catalyzed Addition of Trialkylaluminum Compounds to Epoxides"
Eur. J. Org. Chem. 2001, 4445.
- C. Schneider
"The Silyloxy-Cope Rearrangement of Syn-Aldol Products: Evolution of a Powerful Synthetic Strategy"
Synlett 2001, 1079.
- C. Schneider, M. Hansch
"Zr(OtBu)4-catalysed synthesis of acetone aldol adducts and domino aldol Tishchenko reactions with diacetone alcohol as enol equivalent“
Chem. Comm. 2001, 1218.
- C. Schneider
"Quaternary Ammonium Salt Catalyzed Azidolysis of Epoxides with Trimethylsilyl Azide"
Synlett 2000, 1840.
- C. Schneider, O. Reese
"Diastereoselective Conjugate Additions to tLeucine-Derived N-Enoyl-1,3-oxazolidin-2-ones"
Synthesis 2000, 1689.
- C. Schneider, O. Reese
"Domino-Michael-Aldol- und Domino-Michael-Mannich-Reaktionen. Hochdiastereoselektive Synthese funktionalisierter Cyclohexane"
Angew. Chem. 2000, 112, 3074; Angew. Chem. Int. Ed. 2000, 39, 2948.
C. Schneider, J. Brauner
- "Lewis base catalyzed addition of triethylaluminum to epoxides“
Tetrahedron Lett. 2000, 41, 3043.
- C. Schneider, A. Schuffenhauer
"Stereodivergent Synthesis of Highly Substituted Tetrahydropyrans"
Eur. J. Org. Chem. 2000, 73.
- C. Schneider
"Lewis Acid Reagents (Rezension)"
H. Yamamoto (Hrsg.), Oxford Press, 1999, Angew. Chem. 2000, 112, 834.
- C. Schneider
"New Polyol Syntheses (Book Chapter)"
Organic Synthesis Highlights IV, H.-G. Schmalz (Hrsg.), Wiley-VCH, 2000, 58.
- C. Schneider, M. Rehfeuter
"General and Asymmetric Synthesis of 1,3,5-Triols with Pendant Functional Groups"
Chem. Eur. J. 1999, 5, 2850.
- C. Schneider, C. Börner, A. Schuffenhauer
"Stereoselective Synthesis of Highly Substituted Piperidines"
Eur. J. Org. Chem. 1999, 3353.
- C. Schneider
"Radikale und Radikalionen in der Organischen Synthese (Rezension)"
T. Linker, M. Schmittel, Wiley-VCH, 1998, Nachrichten aus Chemie, Technik und Laboratorium 1999, 47, 1146.
- C. Schneider
"In Memoriam Ulrich Schöllkopf"
Nachrichten aus Chemie, Technik und Laboratorium 1999, 47, 1428.
- C. Schneider
"Application of Transition Metal Catalysts in Organic Synthesis (Rezension)"
L. Brandsma, Springer, 1998, Nachrichten aus Chemie, Technik und Laboratorium 1999, 47, 460.
- C. Schneider
"Die Cope-Umlagerung von Aldolprodukten"
Habilitationsschrift, Göttingen, 1998.
- C. Schneider
"Application of the Silyloxy-Cope Rearrangement of Chiral Aldol Products Towards a Synthesis of (+)-Lasiol"
Eur. J. Org. Chem. 1998, 1661.
- C. Schneider, C. Börner
"Novel and Stereocontrolled Synthesis of Enantiopure and Polyalkylsubstituted Piperidines"
Synlett 1998, 652.
- C. Schneider, M. Rehfeuter
"Enantioselective Polyol Synthesis via the Cope Rearrangement of Chiral Aldol Products. A Synthesis of the C1-C10-Fragment of Nystatin A1"
Tetrahedron Lett. 1998, 39, 9.
- C. Schneider
"Neue Polyol-Synthesen"
Angew. Chem. 1998, 110, 1445; Angew. Chem. Int. Ed. 1998, 37, 1375.
- C. Schneider
"Organische Chemie in Goslar ‑ 2. Deutsch-Italien. Symposium (Tagungsbericht)"
Nachrichten aus Chemie, Technik und Laboratorium 1997, 45, 994.
- C. Schneider
"Stereodivergent Synthesis of Enantiopure Tetrahydropyrans via the Silyloxy-Cope Rearrangement of Chiral Aldol Products"
Synlett 1997, 815.
- C. Schneider, M. Rehfeuter
"Highly Stereoselective Cope Rearrangements of Enantiomerically Pure Silylated Syn-Aldols"
Tetrahedron 1997, 53, 133.
- L. F. Tietze, C. Schneider
"Stereodivergent Hetero Diels-Alder Reactions of Chiral 1-Oxa-1,3-butadienes through a Conformational Switch induced by Lewis Acids"
Chem. Eur. J. 1996, 2, 139.
- C. Schneider, M. Rehfeuter
"Stereoselective Cope Rearrangements of Syn- and Anti-Aldol Products"
Synlett 1996, 212.
- L. F. Tietze, C. Schneider
"Ethyl Nitroacetate"
Encyclopedia of Reagents in Organic Synthesis (Hrsg.: L. A. Paquette, S. E. Denmark), Wiley, London, 1995, Vol. 4, 2501.
- L. F. Tietze, C. Schneider
"Diethyl Oxomalonate"
Encyclopedia of Reagents in Organic Synthesis (Hrsg.: L. A. Paquette, S. E. Denmark), Wiley, London, 1995, Vol. 3, 1837.
- L. F. Tietze, A. Montenbruck, C. Schneider
"De Novo Synthesis of Enantiopure Carbohydrates: Preparation of Ethyl b-D- and b-L-Mannopyranosides by an Asymmetrically Induced Hetero Diels-Alder Reaction"
Synlett 1994, 509.
- J. Henkelmann, L. F. Tietze, C. Schneider
"Verfahren zur Herstellung von a,b-ungesättigten g-Oxycarbonsäurehalogeniden",
DE-A14328060, 17.3.94.
- L. F. Tietze, C. Schneider, A. Montenbruck
"Asymmetrically 1,6-Induced Hetero Diels-Alder Reaction of Chiral Oxabutadienes Towards the De Novo Synthesis of Enantiomerically Pure Carbohydrates: Reversal of Diastereofacial Selectivity through Change of Lewis Acid"
Angew. Chem. 1994, 106, 1031; Angew. Chem., Int. Ed. Engl. 1994, 33, 980.
- E. Pohl, R. Herbst-Irmer, M. Noltemeyer, C. Schneider, L. F. Tietze
"The Crystal Structures of endo- and exo-3-Acetoxy-2,4-di-ethoxy-6-(2-oxo-1,3-oxazolidinecarbonyl)-3,4-dihydro-pyran"
Acta Cryst. 1993, C49, 1850.
- L. F. Tietze, C. Schneider, M. Pretor
"Improved Synthesis of (E)-3-Alkoxy- and (E)-3-Phenoxyacryloyl Chlorides"
Synthesis 1993, 1079.
- L. F. Tietze, C. Schneider
"Efficient Control of the Endo/Exo-Selectivity in Intermolecular Hetero Diels-Alder Reactions of a New 1-Oxa-1,3-butadiene with Different Lewis Acids"
Synlett 1992, 755.
- L. F. Tietze, C. Schneider
"Enantioselective Total Synthesis of the Mycotoxin Talaromycin B by a Hetero Diels-Alder Reaction"
J. Org. Chem. 1991, 56, 2476.
![Abbildung basierend auf der Publikation von R. Sarkar, I. Kallweit, C. Schneider; Org. Lett. 2022, 24, 35, 6433–6437, Abb.: Marcel Sickert. zur Vergrößerungsansicht des Bildes: Abbildung zeigt die Brønsted-Säure-katalysierte [6 + 2]-Cycloaddition von transienten 3-Methid-3H-pyrrolen mit 2-Vinylindolen](/fileadmin/_processed_/8/b/csm_Abstractsbild_Publikation_Rahul_OrgLett_2022-15X_01_a8abd01ebf.png)
![Abbildung basierend auf der Publikation von F. Sachse, C. Schneider Adv.Synth.Catal.2021, Abb.: Marcel Sickert zur Vergrößerungsansicht des Bildes: Die Abbildung zeigt die Synthese von Thiazolo[3,4-a]indolen via (3+2)-Cycloaddition von Thioketonen und Indol-2-carbinolen.](/fileadmin/_processed_/d/f/csm_Abstractsbild_Publikation_Florian_Adv_01_49c9568221.png)
![Abbildung basierend auf der Publikation von F. Sachse, C. Schneider Org. Lett. 2021, 23, 2682–2686, Abb.: Marcel Sickert zur Vergrößerungsansicht des Bildes: Abbildung zeigt die Kooperative Photo-induzierte-/Brønsted Säure-katalysierte Cycloaddition von in-situ erzeugten Thioaldehyden und ortho-Chinonmethiden zur Synthese von Benzo[e][1,3]oxathiinen](/fileadmin/_processed_/0/1/csm_Abstractsbild_Publikation_Florian_OrgLett2021-143_1a08494c37.png)
![Abbildung basierend auf der Publikation von I. Kallweit, M. Laue, C. Schneider; Org. Lett. 2020, 22, 9065–9070, Abb.: Marcel Sickert zur Vergrößerungsansicht des Bildes: Abbildung zeigt die Brønsted-Säure-katalysierte (3+2)-Cycloanellierung von in-situ gebildeten 3-Methid-3H-pyrrolen: Asymmetrische Synthese von Cyclopenta[b]pyrrolen](/fileadmin/_processed_/5/e/csm_Abstract_Isa_OrgLett-2020-139_876db7cf92.png)
![Abbildung basierend auf der Publikation von Angew. Chem. 2020, 132, 5580-5585, Abb.: Marcel Sickert zur Vergrößerungsansicht des Bildes: Abbildung zeigt die Kooperative Katalyse für die hochdiastereo- und enantioselektive [4+3]-Cycloanellierung von ortho-Chinonmethiden mit Carbonylyliden](/fileadmin/_processed_/c/c/csm_Abstractbild_Arun-Henning_Angew2020-133_e65537db7f.png)
![Abbildung basierend auf der Publikation von I. Kallweit, C. Schneider; Org. Lett. 2019, 21, 519-523, Abb.: Marcel Sickert. zur Vergrößerungsansicht des Bildes: Abbildung zeigt die Brønsted Säure-katalysierte [6+2]-Cycloaddition von 2-Vinylindoles mit in-situ generierten 2-Methid-2H-pyrrolen zur direkten, stereoselektiven Synthese von 2,3-Dihydro-1H-pyrrolizinen.](/fileadmin/_processed_/d/e/csm_Abstractbild_Publikation_Isa_OrgLett2019-129_6f3742b993.png)